L’holobionte, une nouvelle dimension pour la sélection porcine ?
L’intérêt grandissant pour le rôle du microbiote dans les performances de son hôte réinterroge les méthodes mises en œuvre pour l’amélioration génétique des animaux d’élevage. L’approche holistique qui prend en compte les influences réciproques et les covariabilités entre l’hôte et son microbiote offre des pistes pour concevoir la sélection au niveau de l’holobionte, avec comme exemple l’espèce porcine.
Introduction
Le terme « holobionte » désigne un organisme vivant, qualifié d’hôte, et les communautés microbiennes associées à cet hôte, qualifiées de microbiotes. Cette approche holistique permet de considérer ainsi le porc non pas comme un être isolé, mais comme un « super-organisme » où l’hôte et ses microbiotes forment une entité fonctionnelle et interdépendante. Ce concept permet de mettre en lumière les relations complexes et continues entre l’organisme hôte et les microorganismes qui vivent en association avec lui, comme les bactéries, les archées, les virus, les champignons. La formalisation et la reconnaissance de cette échelle biologique ont ouvert la voie à un domaine de recherche appelé hologénomique, qui vise à prendre en compte à la fois les caractéristiques génomiques de l’hôte et celles de ses microbiotes. Le terme hologénome désigne alors l’ensemble de l'information génétique des hôtes et des communautés microbiennes associées. Dans la théorie classique de l’amélioration génétique, le phénotype résulte de l’expression du génome modulée par les conditions environnementales. Il est formulé de manière très simple comme la somme des effets du génome et de l’environnement. Ce formalisme a permis de bâtir des programmes de sélection très performants. Il existe bien entendu des approches différentes qui prennent en compte des interactions, notamment entre l’expression du génome et l’environnement. La prise en compte des congénères est également possible, afin de modéliser des effets de compétition ou de coopération entre individus. Un autre postulat de base de la sélection est qu’un descendant hérite du demi-génome de chacun de ses géniteurs et exprime donc la moyenne du génome de ses deux parents. Des modélisations plus avancées permettent de moduler cette hérédité stricte afin d’intégrer toutes les voies de transmission d’une expression phénotypique d’un parent vers ses descendants, pouvant inclure des marques épigénétiques, de l’apprentissage mais également des microbiotes (David & Ricard, 2019).
La validité conceptuelle des hologénomes (et des holobiontes) repose sur quatre principes résumés par Rosenberg et Zilber-Rosenberg (2018) et repris ici : i) les communautés microbiennes associées à l’hôte sont omniprésentes ; ii) le collectif hôte-microbiote fonctionne comme un individu biologique (holobionte) intégrant le métabolisme de l’ensemble ; iii) de même que le génome de l’hôte est hérité de ses parents, il y a une transmission par contact d’une fraction significative du contenu microbien, donc du métagénome du microbiote, d’une génération à la suivante ; iv) l’hologénome est sujet à des variations génétiques provoquées par une diversité de processus comprenant des mutations de novo et la recombinaison, ainsi que l'acquisition de nouveaux microbes. Les génomes microbiens étant susceptibles d’évoluer plus rapidement que celui de l’hôte, ils peuvent jouer un rôle important voire majeur dans l’adaptation et l’évolution de l’holobionte.
Bien que les communautés microbiennes se répartissent sur de nombreuses parties du corps, internes et externes, elles n’ont pas toutes été étudiées de manière approfondie, et souvent un seul type de microbiote est analysé. Dans la suite de cette revue, bien que quelques résultats soient disponibles sur les microbiotes respiratoire, cutané, vaginal ou séminal, nous ferons surtout référence au microbiote intestinal/fécal. L’une des difficultés est de prélever des échantillons, de préférence de manière peu ou pas invasive. Chez le porc, les fèces offrent une bonne représentativité du microbiote intestinal, même si elles ne reflètent que partiellement sa composition, comme chez les humains. Cette propriété, couplée à la facilité de collecte des fèces, a favorisé l’étude du microbiote intestinal chez le porc. Les préconisations pour préserver les échantillons à –80 °C au moment du prélèvement constituent un des freins à des analyses à plus large échelle mais des alternatives de stockage à température ambiante se développent.
Cette revue fait le point sur l’état des connaissances sur le déterminisme génétique de la composition du microbiote chez le porc, dans une optique d’améliorer la sélection des populations animales pour les caractères influencés conjointement par le génome de l’hôte et son microbiote.
1. Le microbiote intestinal du porc
1.1 La composition du microbiote
La majorité des microbiotes porcins se trouve dans l’intestin, bien que des communautés microbiennes soient présentes dans d'autres parties du corps comme la peau, les muqueuses respiratoires et urogénitales. Ces microbes influencent de nombreuses fonctions vitales de l’organisme porcin, comme la digestion, l’immunité, la régulation métabolique et même le comportement.
Figure créée avec BioRender.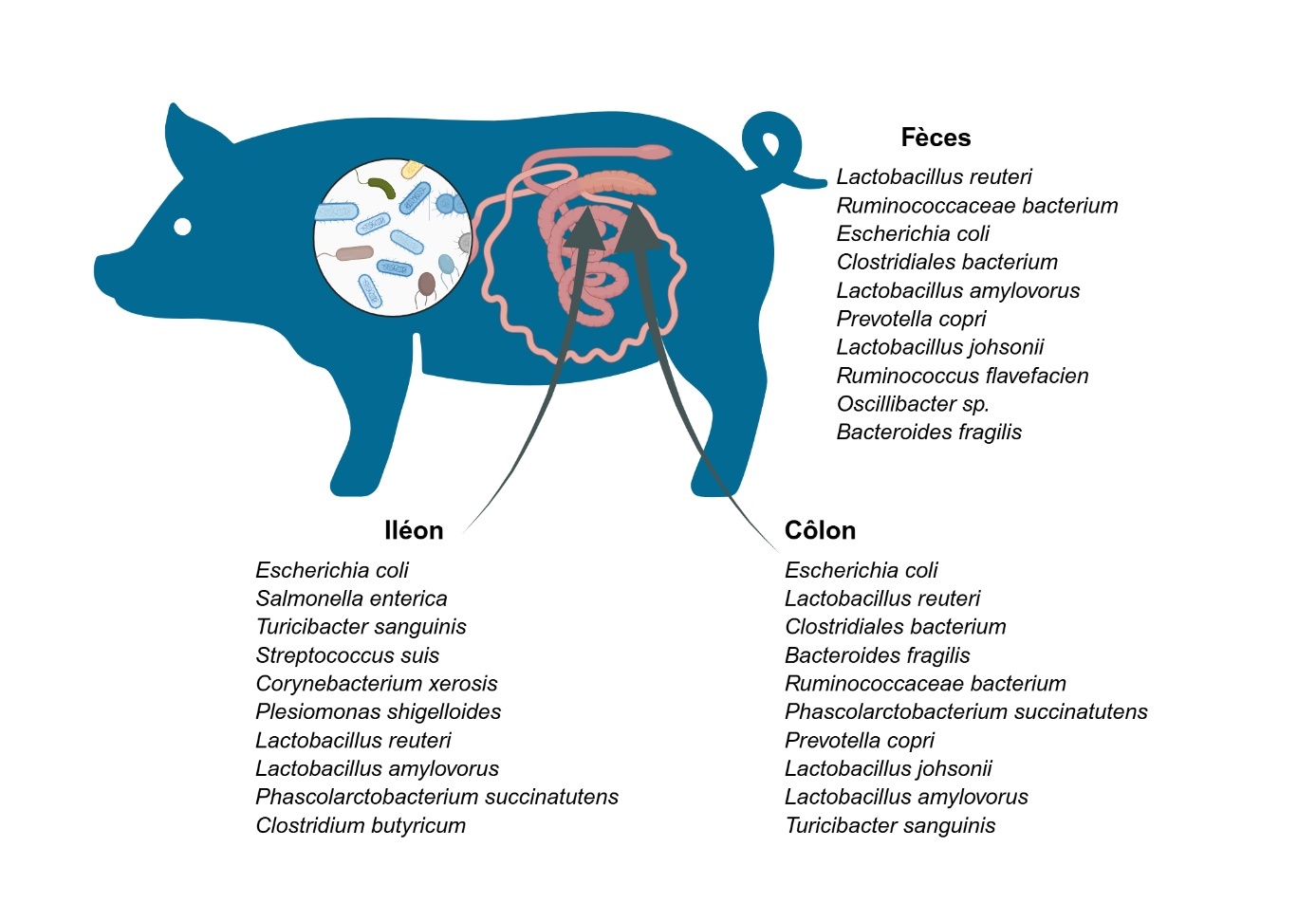
Figure 1. Représentation simplifiée des principaux genres bactériens présents dans les différents segments du tube digestif du porcelet, d’après Huang & Chen (2023).
Le tractus gastro-intestinal des vertébrés est l'un des environnements les plus densément peuplés en microbes, avec environ 1010 à 1011 cellules par gramme de fèces sec (Ley et al., 2006 ; Walker & Hoyles, 2023). Les microorganismes composant le microbiote intestinal résident à l’extérieur de la couche muqueuse et dans les microvillosités. L’intestin n’est pas seulement la plus grande interface entre les environnements externe et interne des animaux, il contient également la plus grande quantité et la plus grande diversité de microorganismes. Le microbiote du tractus digestif est défini comme une communauté écologique composée de microorganismes commensaux, symbiotiques et pathogènes, qui comprend des bactéries, largement dominantes, des archées, des virus, des parasites, des champignons, et des protistes. En raison des technologies mises en œuvre, la plupart des études sur la composition du microbiote se sont focalisées sur la caractérisation et la fonction des bactéries. Les principaux genres bactériens présents chez le porcelet dans différents compartiments intestinaux sont représentés sur la figure 1.
Les populations bactériennes intestinales sont dominées par les Firmicutes et les Bacteroidota ; les autres embranchements représentés comprennent les Proteobacteria, les Actinobacteria, les Fusobacteria, les Verrucomicrobia, les Fibrobacteres et les Spirochaetes (Ley et al., 2008). Les bactéries intestinales et leur hôte vivent dans des relations mutualistes. Le microbiote participe à la digestion, l’utilisation des nutriments, l’élimination des toxines, la protection contre les agents pathogènes et à la régulation des systèmes endocrinien et immunitaire de son hôte. Les microbes qui résident dans l’intestin ont ainsi la capacité de produire des enzymes qui dégradent les polysaccharides alimentaires provenant des parois cellulaires des plantes, ce que les enzymes de l’hôte ne peuvent pas faire (Flint et al., 2008). La fermentation de ces polysaccharides engendre des produits finaux, tels que des acides gras à chaîne courte (AGCC), que l’hôte utilise comme sources nutritionnelles (Martens et al., 2011). La quantité d’énergie fournie par les AGCC produits peut par exemple atteindre 20 à 30 % chez de nombreux animaux omnivores dont le porc (Bergman, 1990).
1.2. Caractérisation du microbiote
L’un des premiers enjeux est de caractériser le microbiote d’un individu. La plupart des études ont utilisé une information partielle basée sur un séquençage réduit de l’ADN microbien. En effet, il est possible d’obtenir la composition d’un microbiote au niveau des genres bactériens en séquençant un même segment du gène de l’ARN ribosomique 16S et en alignant les séquences obtenues sur les séquences annotées présentes dans des bases de référence : RDP (Wang et al., 2007), Greengenes (McDonald et al., 2024), NCBI (Federhen, 2012), SILVA (Quast et al., 2012). Le gène ARNr 16S comporte neuf régions variables intercalées entre des régions conservées. Les régions variables de ce gène sont fréquemment utilisées pour la classification phylogénétique des genres dans diverses populations microbiennes du fait de leur faible vitesse d’évolution. Mais, le plus souvent, elles ne permettent pas de trouver une correspondance jusqu’à l’échelle taxonomique de l’espèce microbienne. Cette méthode de séquençage est applicable sans connaissances préalables du microbiote analysé, quel que soit l’holobionte animal étudié. Ce choix de séquençage partiel est largement utilisé dans les études portant sur le déterminisme génétique des caractères en raison de sa mise en œuvre relativement simple et de son coût modéré. Grâce aux bases de données bien établies et régulièrement enrichies, contenant les informations taxonomiques pour identifier les genres bactériens à partir des séquences 16S et aux programmes informatiques largement partagés, l’analyse des données est simplifiée. Quelques difficultés numériques peuvent cependant apparaître lorsque le nombre d’individus analysés est très élevé. L’une des limites les plus importantes est que les résultats ne sont pas homogènes selon les méthodes utilisées avec une absence de standard garantissant la reproductibilité des résultats au fil du temps, un effet potentiellement plus important pour l’annotation des genres bactériens qui peut évoluer au fil du temps dans les bases de références. Comparer et interpréter les résultats de différentes études doit donc tenir compte de ces éléments.
Le séquençage complet des génomes d’une communauté microbienne (c.-à-d. métagénomique) permet quant à lui de connaître l’ensemble des gènes présents et d’améliorer la résolution taxonomique de la composition du microbiote au niveau des différentes espèces microbiennes, y compris les virus et les eucaryotes. La limite restante est la connaissance a priori de ces espèces ou la réalisation d’un travail préalable d’assemblage de novo. La métagénomique permet également d’identifier les fonctions des bactéries présentes grâce à l’annotation des gènes bactériens. En raison de son coût, elle est moins fréquemment mise en œuvre, au-delà de quelques centaines d’individus chez les animaux d’élevage, contrairement aux études chez les humains. Les catalogues de référence qui répertorient les gènes des organismes du microbiote sont donc indispensables pour étudier le métagénome. Le premier catalogue publié chez le porc, qui contenait 7,7 millions de gènes (Xiao et al., 2016), a été récemment enrichi et en contient maintenant plus de 17 millions (Chen et al., 2021 ; Plaza Oñate et al., 2021).
Quelle que soit la méthode, le comptage des séquences et leur regroupement par séquences similaires permettent de construire des tables d’abondances relatives de variants de séquences d’amplicon (ASV : amplicon sequence variant), d’unités taxonomiques opérationnelles (OTU : operational taxonomic unit), de gènes ou de fonctions de gènes, d’espèces ou de genres voire de familles bactériennes. Les ASV et OTU sont issus du séquençage ciblé (c.-à-d. 16S). L’information sur l’ensemble des gènes, les annotations taxonomiques précises et les fonctions sont obtenues par l’analyse des données métagénomiques, les approches ciblées apportant des prédictions moins fines. Les tables d’abondances relatives permettent de caractériser la diversité des microbiotes, de les comparer entre eux, et de prendre en compte la composition d’un microbiote dans différents modèles d’analyses. Même si peu utilisée en porc, une méthode de quantification absolue combinée à l’approche 16S est possible grâce à l’utilisation de standards internes (Zemb et al., 2020). Selon l’échelle retenue, les abondances relatives peuvent concerner quelques dizaines à quelques milliers de variables. Ramenée au niveau du genre, une table d’abondance peut recenser quelques centaines de variables, avec une proportion importante de genres ayant des abondances relatives très faibles. De par la nature compositionnelle des comptages et des abondances relatives (au sens où les variables sont liées entre elles par construction puisque la somme des variables est constante) et de la surreprésentation des valeurs nulles dans les distributions, des méthodes spécifiques de transformations des variables avant les analyses statistiques sont souvent mises en œuvre (Lin & Peddada, 2020). Les transformations les plus couramment utilisées dans les modélisations génétiques sont de type logarithmique ou log-ratio, en écartant les variables ayant beaucoup (avec une part d’arbitraire) de valeurs nulles. Hormis pour les genres les plus représentatifs, les distributions des variables (même après transformation) respectent rarement les règles de la normalité.
En tant qu’écosystème, un microbiote peut également être caractérisé de manière générique par sa diversité ou sa richesse. Les indicateurs de diversité les plus étudiés sont des indices de diversité alpha, qui correspondent soit au nombre d’espèces présentes : la richesse microbienne et l'estimateur Chao1, soit à l’homogénéité des abondances : l’indice de Shannon et l’indice de Simpson (Haegeman et al., 2013).
1.3. Classification des communautés
Chez les vertébrés, de nombreuses études se sont concentrées sur la décomposition taxonomique du microbiote intestinal. Depuis plus d’une décennie, l’analyse des abondances relatives des genres chez les humains a permis de mettre en évidence que les échantillons peuvent être classés en groupes distincts appelés « entérotypes » (Arumugam et al., 2011). La première étape pour la classification en entérotypes est d’estimer la ressemblance entre chaque individu à partir de la matrice d’abondances. La mesure retenue est la divergence de Jensen-Shannon, souvent utilisée pour comparer des distributions de probabilité. Une fois calculée entre chaque paire d'échantillons, on utilise cette mesure dans une méthode de clustering, pour regrouper les individus en minimisant les différences intragroupes et en maximisant les différences intergroupes.
Plusieurs analyses réalisées sur des porcelets de 60 jours ont révélé et confirmé l'existence de deux entérotypes, dirigés par les genres Prevotella et Mitsuokella (entérotype PM) Ruminococcus et Treponema (entérotype RT) (Mach et al., 2015 ; Ramayo-Caldas et al., 2016 ; Larzul et al., 2024). À des stades différents, d’autres enrichissements de certains genres ont permis de distinguer d’autres entérotypes. Pour des porcelets au sevrage, Lu et al. (2018) ont trouvé deux entérotypes distincts, avec un entérotype enrichi en Prevotella et un autre enrichi en Escherichia. Dans différentes conditions d’élevage commercial, une étude a montré qu’autour du sevrage, quatre entérotypes ont pu être identifiés, avec des enrichissements respectifs en Prevotella, Faecalibacterium, Roseburia, et Lachnospira (Luise et al., 2021). Les méthodes de regroupement utilisées pour caractériser les entérotypes ont contribué à la compréhension de la diversité du microbiote intestinal des porcs. Cependant, l’appartenance à un entérotype est une donnée relative à la population étudiée, elle peut donc varier au cours du temps. De plus, pour comprendre les relations entre le microbiote et son hôte, la description du microbiote par une variable binaire (par exemple entérotype RT ou PM) peut être trop réductrice.
La classification par entérotype n’est pas la seule méthode de classification ou de partition proposée dans la littérature, mais ces approches alternatives ont été peu mises en œuvre chez le porc, hormis par Vourlaki et al. (2025). En s’appuyant sur le concept d’entérosignature, défini comme une signature microbienne de communautés bactériennes co-occurrentes (Frioux et al., 2023), le microbiote peut être représenté par une combinaison de différentes guildes bactériennes.
Le nom de l’entérosignature (ES) est donné par le genre prédominant (Prev = Prevotella, Trep = Treponema, Lact = Lactobacillus, Clos = Clostridium, Stre = Streptococcus) (d’après Vourlaki et al., 2025).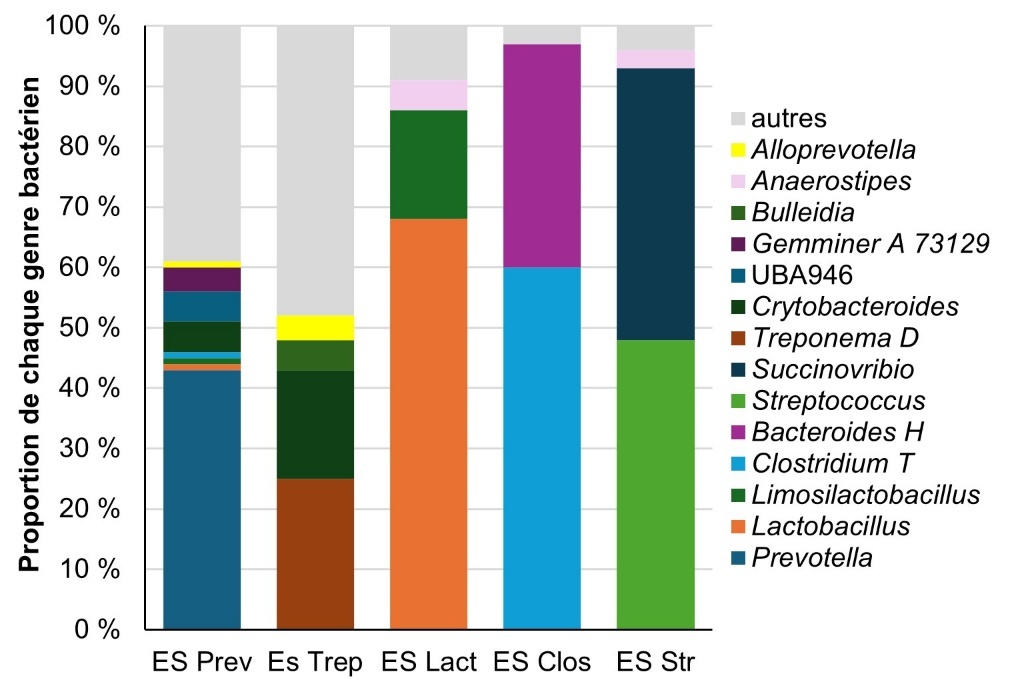
Figure 2. Représentation des entérosignatures identifiées chez des porcelets de 60 jours d’âge, avec le pourcentage des genres bactériens constituant chacune des entérosignatures.
Vourlaki et al. (2025) ont ainsi décrit cinq entérosignatures chez le porc à 60 jours, dominées par six genres différents : Prevotella, Streptococcus, Succinovibrio, Lactobacillus, Clostridium, et Treponema (figure 2). Ces entérosignatures évoluent avec l’âge puisqu’à 190 jours, quatre entérosignatures sont identifiées, dont trois présentes à 60 jours (Prevotella, Lactobacillus et Streptococcus) et une nouvelle dominée par UAB2810. Si la signification n’est pas totalement équivalente entre les entérotypes et les entérosignatures, les genres Prevotella et Treponema ont une importance pour différencier deux types de communautés bactériennes mutuellement exclusives l’une de l’autre. De plus, le poids à 60 jours est positivement corrélé avec la proportion de l’entérosignature dominée par Prevotella comme il a été montré que l’entérotype PM est associé à une meilleure vitesse de croissance post-sevrage estimée entre 28 et 70 jours d’âge (Ramayo-Caldas et al., 2016). S’il a été montré que l’entérotype PM est associé à une moindre richesse du microbiote, le lien entre entérosignature et diversité du microbiote n’a pas été exploré.
Même si cela n’a pas encore été réalisé chez le porc, il est tout à fait envisageable d’étendre ce type de classifications à des microbiotes autres que le microbiote intestinal.
2. Influence de la génétique de l’hôte sur la composition du microbiote
2.1. Comparaison de génotypes
Comprendre l’influence génétique de l’hôte sur l’implantation et l’évolution des microbiotes est complexe. Cela repose sur la mesure d’un grand nombre d’individus dans des conditions homogènes, de préférence contrôlées. Deux approches complémentaires peuvent être mises en œuvre pour explorer la variabilité génétique de l’hôte pour les caractéristiques du microbiote.
La première approche est la comparaison de races ou de croisements de races. Les comparaisons entre races ou croisements de races élevés dans les mêmes conditions sur des effectifs qui dépassent quelques dizaines d’individus sont peu fréquentes. En comparant trois races porcines, Duroc, Landrace et Large White, à trois âges différents pendant la période de croissance, Bergamaschi et al. (2020b) ont montré que les compositions des microbiotes étaient différentes entre ces races. Le résultat mis en avant par les auteurs est une différence positive de diversité du microbiote entre les Landrace d’une part et les Duroc ou Large White d’autre part. De plus, quel que soit l’âge, le microbiote des porcs de race Duroc présentait une proportion supérieure des genres Catenibacterium et Clostridium alors que les Landrace avaient des proportions de Bacteroides plus élevées que les Large White. Le détail des différences entre races montre qu’au-delà de ces grandes lignes, la composition du microbiote de chaque race et les différences entre races évoluent largement en fonction de l’âge. Sans que le nombre total d’ASV ne soit mentionné dans l’étude, il y a environ 400 ASV avec des abondances relatives significativement différentes entre les races comparées deux à deux. La race a donc un effet sur la composition du microbiote et ces résultats mériteraient d’être confortés par d’autres études similaires pour mieux évaluer l’importance de ces différences en lien avec l’histoire de la sélection et les caractéristiques actuelles de ces races.
La deuxième approche est la comparaison de lignées sélectionnées expérimentalement sur un caractère, par exemple l’efficience alimentaire. Si le caractère est corrélé génétiquement aux caractéristiques du microbiote, la sélection va entraîner des différences sur le profil des microbiotes entre les lignées sélectionnées. L’absence de différence ne signifie pas que la génétique de l’hôte n’a pas d’incidence sur le microbiote, mais que le caractère sélectionné n’est pas lié au microbiote ou que le nombre d’individus étudiés n’est pas suffisamment important pour mettre en évidence des différences de faible amplitude.
Dans diverses espèces, il existe plusieurs expériences de sélection sur l'efficacité alimentaire ou sur des caractères associés tels que la digestibilité. Compte tenu des liens, souvent mis en évidence, entre le microbiote intestinal et l'efficacité alimentaire ou digestive, la comparaison de lignées divergentes contribue à explorer le déterminisme génétique du microbiote du tube digestif et l’importance respective de l’hôte et du microbiote. Aliakbari et al. (2021) ont par exemple mis en évidence des différences dans les abondances relatives de quelques dizaines de genres entre le microbiote fécal de lignées sélectionnées de manière divergente sur l’efficacité alimentaire résiduelle. Le nombre de genres initialement identifiés pour l’ensemble des animaux était de 298, avec seulement 75 genres étudiés, présents chez au moins 80 % des individus. La lignée la plus efficace, par rapport à la lignée la moins efficace, est enrichie pour 42 genres, dont Clostridium_sensu_stricto_1, Prevotella_7 et Terrisporobacter, et appauvrie en 10 genres tels que Lactobacillus, Prevotella_9 et Streptococcus. Les différences, entre lignées, d’abondance relative des genres sont généralement de quelques pourcents, hormis pour Lactobacillus avec une abondance relative deux fois moins élevée dans la lignée la plus efficace (10,1 % vs 20,9 %). L'enrichissement d'un plus grand nombre de genres pour la lignée la plus efficace par rapport à la lignée la moins efficace a également été mis en évidence dans la même expérience de sélection (Kubasova et al., 2018), mais sur un plus petit nombre d'individus (N = 36 par lignée) incluant Clostridium_sensu_stricto pour la lignée la plus efficace et Lactobacillus pour la lignée la moins efficace. Sur la liste des genres plus ou moins abondants dans l’une ou l’autre lignée, à part les deux genres mentionnés ci-dessus, il y a peu de consensus entre les deux études. Ceci peut s'expliquer, entre autres, par des âges de mesure différents. L’étude de Kubasova et al. (2018) montre également une interaction entre la lignée et le stress sanitaire, ce qui suggère que, selon les conditions d’élevage, les différences entre lignées peuvent être modulées.
2.2. Héritabilité de la composition du microbiote
a. Héritabilité des abondances relatives des genres bactériens
Plusieurs études se sont intéressées à l’estimation des valeurs d’héritabilité de la composition du microbiote intestinal, afin d’évaluer l’influence de la génétique de l’hôte sur les abondances relatives des genres bactériens.
Il est relativement difficile de synthétiser les résultats en raison de la diversité des conditions de prélèvements, notamment l’âge, et les méthodes employées pour identifier les genres bactériens. À la naissance, le microbiote du porcelet est influencé par celui de sa mère, lui-même fonction du statut sanitaire de l’élevage et de la santé de la truie. À la suite du sevrage, le microbiote largement dominé par Lactobacillus pendant la phase d’allaitement change avec une domination progressive de Prevotella (Mach et al., 2015 ; Borey et al., 2022). Pour un sevrage vers 28 jours, le microbiote du porcelet se stabilise à environ 36 jours (Mach et al., 2015). À un stade plus avancé, en engraissement, l’âge semble moins influencer la composition du microbiote que les pratiques d’élevage ou l’alimentation.
L’un des facteurs importants de la valeur des héritabilités des abondances relatives des genres bactériens semble être l’âge (Larzul et al., 2024). Par exemple, chez des porcelets d’environ 60 jours d’âge, l’héritabilité de quelques genres bactériens, notamment, Prevotella, Treponema, Ruminococcus et Mitsuokella est de l’ordre de 0,3. Quelques genres ont même une héritabilité supérieure, de l’ordre de 0,4 (Terrisporobacter, Dialister et Campylobacter). Pour les mêmes genres bactériens que les quatre premiers mentionnés, des héritabilités inférieures à 0,2 ont été estimées pour des animaux âgés d’environ 300 jours (Chen et al., 2018) ou 110 jours (Déru et al., 2022a). Cependant, aux âges les plus élevés, huit genres ont été trouvés avec une valeur d’héritabilité de l’ordre de 0,3. Pour des prélèvements réalisés post-mortem dans le côlon de porcs de race Piétrain (Camarinha-Silva et al., 2017), des héritabilités moyennes (h² = 0,32) à élevées (h² = 0,57) ont été estimées pour huit genres. Dans le cas de l’étude de Déru et al. (2022a), il est intéressant de mentionner que, malgré des différences de régimes alimentaires, avec un aliment plus fibreux donné à une partie des porcs dans la phase d’engraissement, les valeurs d’héritabilité sont peu affectées par ce facteur de variation, les porcs étant par ailleurs élevés dans les mêmes conditions. Aliakbari et al. (2021) ont également publié des héritabilités supérieures à 0,3 pour plusieurs genres bactériens caractérisant le microbiote de porcs âgés de 15 semaines, parmi lesquels Clostridium_sensu_stricto_1 (h² = 0,5), Blautia, Terrisporobacter ou encore Mitsuokella. Pour des porcelets en allaitement (Yang et al., 2022), les valeurs d’héritabilités sont faibles voire nulles. De même, pour des porcelets mesurés à plusieurs stades, les valeurs d’héritabilité sont les plus faibles pour les porcelets au sevrage, alors qu’à des âges plus tardifs, les héritabilités de quelques familles (Peptostreptococcaceae, Clostridiaceae) peuvent dépasser 0,4 (Bergamaschi et al., 2020a). On peut supposer qu’à des âges très précoces, la composition du microbiote, largement influencée par l’allaitement maternel et l’environnement périnatal, n’est pas encore l’expression de la génétique de l’hôte, mais plutôt celle de l’environnement microbien immédiat (Tancredi et al., 2025). Avant sevrage, le système n’est pas encore stable, il évolue chaque jour avec probablement de fortes variabilités inter-individuelles.
L’étude du microbiote intestinal a été privilégiée car il est en lien avec de multiples fonctions importantes en élevage (digestion, immunité, résistance aux pathogènes…), et jusqu’à présent peu d’études se sont intéressées aux autres microbiotes. Certaines études ont analysé l’influence du microbiote vaginal notamment sur la reproduction, dont une d’un point de vue génétique. Cette étude s’est intéressée au microbiote vaginal des cochettes, en lien avec la réponse vaccinale au syndrome dysgénésique et respiratoire du porc et aux performances de reproduction (Sanglard et al., 2020). Le microbiote vaginal a été prélevé quatre jours (J4) puis 52 jours (J52) après la vaccination. L’héritabilité des abondances relatives des OTU était généralement un peu plus élevée à 52 jours qu’à quatre jours, et variait de 0 à 0,60 (Fusobacterium) à J4 et de 0 à 0,63 (Terrisporobacter) à J52, avec des répétabilités entre les deux prélèvements plutôt faibles mais pouvant atteindre des valeurs de l’ordre de 0,6.
b. Héritabilité des indices de diversité
Une manière simple pour aborder l’influence de la génétique de l’hôte sur la composition du microbiote intestinal est de s’intéresser aux indices de diversité ou de richesse qui permettent de regarder une information synthétique, que ce soit en termes d’héritabilités ou de relations avec les phénotypes. Plusieurs études ont confirmé que la richesse et la diversité du microbiote augmentent avec l’âge (Ke et al., 2019 ; Wang et al., 2019 ; Maltecca et al., 2020).
Pour des animaux mesurés à plusieurs âges successifs, Lu et al. (2018) ont montré que l’héritabilité de la diversité alpha et la richesse tendent à s’accroître avec l’âge, avec des valeurs particulièrement faibles au sevrage (< 0,05), modérées à la semaine 15 (0,15 à 0,26) et jusqu’à 0,33 en fin d’engraissement. Des valeurs d’héritabilité de l’ordre de 0,2 pour les indices de diversité alpha ont également été estimées pour des porcs de 15-16 semaines d’âge (Aliakbari et al., 2021 ; Déru et al., 2022a). En période de post-sevrage, à 60 jours d’âge, la valeur d’héritabilité pour ce même indice peut être encore plus élevée (h² = 0,36) (Larzul et al., 2024).
Une seule étude a rapporté des estimations d’héritabilité d’indices de diversité pour un microbiote différent du microbiote intestinal chez le porc, en l’occurrence le microbiote vaginal des cochettes, avec des valeurs faibles de l’ordre de 0,1 (Sanglard et al., 2020).
c. Héritabilité des entérotypes/entérosignatures
Il existe quelques valeurs estimées pour les communautés bactériennes décrites par des entérotypes ou par des entérosignatures. La valeur d’héritabilité pour les entérotypes (classés en RT/PM) des porcelets de 60 jours est modérée (h² = 0,3) (Larzul et al., 2024), du même ordre de grandeur que les héritabilités des genres bactériens qui constituent les taxons-clés de ces entérotypes. Pour les entérosignatures, les valeurs d'héritabilité dépendent de la communauté bactérienne (Vourlaki et al., 2025), la plus élevée étant estimée à 0,36 pour l’entérosignature dominée par Treponema et la moins élevée à 0,24 pour les deux entérosignatures dominées par Streptococcus ou Clostridium.
2.3. Marqueurs génétiques et gènes
Huang et Chen (2023) ont réalisé une synthèse des résultats de six études d’association sur la composition du microbiote fécal ou intestinal chez le porc (Chen et al., 2018 ; Crespo-Piazuelo et al., 2019 ; Bergamaschi et al., 2020a ; Ramayo-Caldas et al., 2020 ; Reverter et al., 2021 ; Yang et al., 2022) ou vaginal (Sanglard et al., 2020). Toutes ces études ont permis de détecter des marqueurs génétiques ayant un effet sur les abondances relatives de genres bactériens, et la plupart ont proposé des gènes candidats proches des marqueurs identifiés.
Les gènes liés au système immunitaire, tels que ceux impliqués dans la production de cytokines, d’anticorps et de récepteurs Toll-like, peuvent être particulièrement importants (Reverter et al., 2021). Ils influencent la manière dont l’hôte porcin reconnaît les microbes et module ses réponses immunitaires en fonction des microbes bénéfiques ou pathogènes présents dans son environnement. Même si cela n’a pas encore été formellement démontré, on peut considérer que le polymorphisme des gènes associés à l’immunocompétence des porcs affecte la composition du microbiote intestinal, favorisant certaines espèces microbiennes bénéfiques tout en limitant la croissance d’autres potentiellement nuisibles pour assurer l’implantation et la durabilité d’un microbiote sain.
Yang et al. (2022) sont allés jusqu’à l’identification d’un gène du porc influant le microbiote intestinal. Une analyse fine d’une zone du chromosome 1, ayant un effet sur l’abondance de Erysipelotrichacea a permis d’identifier une délétion de 2,3 kb dans le gène ABO (alpha 1–3-N-acetylgalactosaminyltransferase) comme mutation causale. Ce gène ajoute une N-acétylgalactosamine aux glucoprotéines de la muqueuse intestinale et des cellules sanguines. La délétion de 2,3 kb du gène ABO entraîne l’incapacité d’ajouter de la N-acétylgalactosamine (GalNAc) aux mucines hautement glycosylées du mucus intestinal. Cela a conduit à des concentrations intestinales réduites de GalNAc chez les individus présentant le génotype délété, et a donc réduit la croissance de certaines espèces d’Erysipelotrichaceae utilisant la GalNAc comme source de carbone. Un autre exemple concerne la délétion du gène porcin MSTN qui entraîne une recomposition du microbiote intestinal enrichi en bactéries productrices d’acides gras à chaîne courte (AGCC). Ces modifications favorisent la croissance des fibres musculaires glycolytiques rapides par l’élévation des niveaux d’AGCC, en particulier l’acide valérique, qui active la voie Akt/mTOR et atténue l’atrophie musculaire (Luo et al., 2023).
3. Influence de la variabilité du microbiote sur les phénotypes
Le rôle du microbiote sur les caractères de l’hôte est de plus en plus documenté, les études s’intéressant aux mécanismes de dialogues entre les différentes entités. Dans cette partie, nous nous intéressons plus particulièrement au déterminisme génétique de ces interactions. Le microbiote intestinal affecte de manière significative plusieurs phénotypes de l’hôte porcin. Ces effets sont principalement observés dans des domaines tels que la croissance, le métabolisme énergétique et la réponse immunitaire. Le microbiote influence également les réponses immunitaires locales et systémiques. Des bactéries spécifiques dans l’intestin peuvent moduler la production de cytokines et d’autres molécules de signalisation immunitaire. Par exemple, un microbiote riche en Lactobacilles et bifidobactéries est associé à une meilleure santé intestinale et à une réduction de l’inflammation chronique, un facteur souvent lié à la santé et au bien-être des porcs. Des déséquilibres dans la composition du microbiote (appelés dysbioses) peuvent être liés aux maladies métaboliques ou inflammatoires. Le microbiote peut agir sur la perméabilité intestinale, empêchant ainsi le passage des toxines ou agents pathogènes dans la circulation sanguine. Ces quelques exemples, loin de l’exhaustivité, montrent à quel point comprendre les fonctions du microbiote est essentiel pour servir de leviers et moduler les caractéristiques de l’hôte.
3.1. Corrélations génétiques avec les caractères d’intérêt de l’hôte et la composition du microbiote
En considérant la composition du microbiote comme un caractère de l’hôte, il est possible d’estimer des corrélations génétiques entre les caractéristiques de la composition du microbiote et les phénotypes de l’hôte. Il est difficile de faire une véritable synthèse des corrélations génétiques estimées dans différentes études entre des abondances relatives (au niveau des OTU/ASV ou au niveau des genres) à cause des variations de méthodes et de conditions de mesures. De plus, compte tenu des effectifs étudiés, les corrélations ne sont estimées qu’avec les genres les plus héritables (quelques dizaines voire moins) et avec une précision limitée. Les résultats présentés peuvent cependant donner un aperçu des évolutions potentielles de la composition du microbiote en fonction des caractères sélectionnés.
Aliakbari et al. (2021) ont estimé des corrélations génétiques entre les abondances des genres bactériens du microbiote fécal prélevé vers la fin de l’engraissement et des caractères de croissance, d’efficacité alimentaire et de composition corporelle. Les corrélations génétiques les plus élevées, en valeur absolue, ont été estimées avec l’épaisseur de gras et la consommation moyenne journalière. Aucune corrélation génétique (rg) n’était significative avec le gain moyen quotidien ou l’indice de consommation. Dans une autre étude (Déru et al., 2022a), l’estimation des corrélations génétiques a permis de dégager deux groupes de genres bactériens, avec des abondances favorablement et significativement corrélées avec les caractères d’efficacité digestive et d’efficacité alimentaire pour 29 genres, ou défavorablement corrélées avec l’efficacité digestive pour 14 genres bactériens. Dans ces deux études, l’augmentation des abondances relatives des genres Shuttleworthia, Desulfovibrio Rikenellaceae_RC9_gut_group et la diminution de l’abondance relative de Faecalibacterium auraient des conséquences favorables sur la composition corporelle et/ou sur les caractères d’efficacité.
Dans l’étude de Déru et al. (2022a), les corrélations génétiques entre genres bactériens ont également été estimées. Sans rentrer dans les détails, les corrélations montrent une structuration assez forte du microbiote avec la présence de groupes de genres antagonistes, notamment entre, d’une part, Prevotella et, d’autre part, Ruminococcus et Treponema. Larzul et al. (2024) ont estimé des corrélations génétiques positives entre l’abondance relative des genres Prevotella et Mitsuokella avec la croissance post-sevrage chez les porcelets âgés de 60 jours et des relations génétiques négatives entre ce caractère et les abondances relatives des genres Treponema et Ruminococcus.
Les corrélations génétiques avec les indices de diversité ont également été estimées, permettant d’utiliser une information synthétique plus facile à appréhender pour estimer les relations génétiques entre le microbiote et les caractéristiques phénotypiques de l’hôte. En engraissement, les indices de diversité sont génétiquement corrélés négativement à la vitesse de croissance ou à l’efficacité alimentaire (Aliakbari et al., 2021 ; Déru et al., 2022a) et positivement à l’efficacité digestive (Déru et al., 2022a). Les indices de diversité sont également négativement corrélés à la vitesse de croissance en post-sevrage. Autrement dit, le microbiote moins divers de l’entérotype PM est plus bénéfique pour des caractères de production comme la croissance chez le jeune que le microbiote de l’entérotype RT, pourtant plus divers (Larzul et al., 2024). Des corrélations génétiques négatives ont également été estimées entre le poids à 60 jours et les entérosignatures dominées par Treponema (rg = –0,43) ou Streptococcus (rg = –0,85), ce qui est cohérent avec la corrélation négative entre Treponema et la croissance post-sevrage (Vourlaki et al., 2025).
3.2. Microbiabilité
La microbiabilité, telle qu'elle a été définie pour la première fois par Difford et al. (2016), permet une vision holistique de l’influence du microbiote sur les caractéristiques de l’hôte. Le concept de microbiabilité a été proposé comme un moyen d’inclure la composition microbienne globale dans la variation phénotypique tout en tenant compte des relations entre les hôtes et leur profil microbien. Comme l’héritabilité (h²) est la proportion de variance expliquée par la génétique de l’hôte, la microbiabilité (m²) est la proportion de variance expliquée par la composition microbienne. De manière formelle, on peut écrire une extension du modèle P = G + E (où le phénotype est la combinaison des effets génétiques et de l’environnement) comme P = G + M + E (où M représente le microbiote). L’idée est donc de modéliser l’effet d’un profil microbien individuel avec un modèle linéaire mixte standard en utilisant une matrice de « relation » microbienne obtenue à partir de l’abondance des OTU pour chaque individu de manière similaire à la matrice de relation génomique. À ce stade, les interactions entre la génétique de l’hôte et l’environnement ne sont pas prises en compte dans les modèles.
Les estimations de microbiabilité ont été réalisées principalement pour les caractères de croissance et d’efficacité alimentaire (Camarinha-Silva et al., 2017 ; Aliakbari et al., 2022 ; Déru et al., 2022b), d’efficacité digestive (Verschuren et al., 2020 ; Déru et al., 2022b), de composition de carcasse et de qualité de viande (Khanal et al., 2021 ; He et al., 2022), et des paramètres immunitaires (Ramayo-Caldas et al., 2021 ; Calle-García et al., 2023). Les estimations de la microbiabilité sont en général faibles à modérées, de l’ordre de 0,1-0,2, pour l’efficacité alimentaire et les caractères de composition de carcasse et de qualité de viande (Camarinha-Silva et al., 2017 ; Aliakbari et al., 2022), élevées pour l’efficacité digestive (> 0,44) et proches de 0 pour la croissance et la composition corporelle (Aliakbari et al., 2022). Dans des conditions d’élevage différentes, l’utilisation d’un régime alimentaire plus fibreux peut augmenter la part de variance expliquée par le microbiote fécal, avec des microbiabilités pouvant atteindre 0,68 pour l’efficacité digestive contre 0,44 avec un aliment standard (Déru et al., 2022a). Afin d’explorer comment les caractéristiques microbiennes et génétiques influencent la variance phénotypique des caractères, les valeurs de microbiabilité et d’héritabilité sont souvent comparées dans la littérature. Cette comparaison s’effectue en incluant l’information génétique et microbienne dans des modèles linéaires mixtes de manière séparée (P = G + E vs P = M + E) ou combinée (P = G + M + E). Dans un modèle incluant à la fois l’effet de la génétique et du microbiote, les microbiabilités pour l’efficacité alimentaire restent inférieures aux valeurs d’héritabilité pour la croissance (0,17 vs 0,26) ou l’efficacité alimentaire (0,35 vs 0,44). En revanche pour l’efficacité digestive, la variance phénotypique est expliquée en partie par la génétique de l’hôte (h² < 0,32), mais surtout par la composition du microbiote intestinal (m² > 0,44) (Déru et al., 2022b). En effet, l’activité de fermentation de la population microbienne dans le gros intestin peut affecter significativement ce caractère. Pour les caractères de la réponse immunitaire, l’héritabilité et la microbiabilité ont montré des valeurs similaires pour 21 caractères immunitaires (Ramayo-Caldas et al., 2021) à l’exception des IgM et IgG (h² > m²) et l’haptoglobine (m² > h²). Dans une étude reprenant les mêmes données sur un sous-ensemble de six caractères immunitaires, les microbiabilités étaient estimées avec des valeurs faibles (0,1 pour les γδ T cells) à moyenne (0,4 pour la concentration sérique en haptoglobine) (Calle-García et al., 2023). Les microbiabilités pour les caractères de qualité de viande sont pour la plupart très faibles (< 0,1) et faibles à modérées pour les caractères de carcasse (> 0,2 pour la croissance estimée à partir du poids de carcasse et le poids de poitrine), en prenant en compte le microbiote fécal caractérisé en cours ou en fin d’engraissement (Khanal et al., 2021).
Le microbiote caractérisé au sevrage conduit à des microbiabilités nulles pour ces caractères de qualité de viande et de carcasse. Les microbiabilités des caractères de mise bas, estimées avec le microbiote vaginal, sont faibles, et en général plus faibles que les héritabilités (Sanglard et al., 2020). La composition de microbiote vaginal explique une part plus importante que la génétique pour le nombre de porcelets sevrés (m² = 0,15) et la mortalité en allaitement (m² = 0,09). Il faut souligner que, dans cette étude, il n’a pas été possible, pour des raisons de convergence du modèle, de prendre en compte simultanément les effets génétiques et les effets du microbiote. En pré-ajustant les phénotypes pour l’effet aléatoire animal, les estimations de m² étaient plus ou moins égales à zéro, montrant que le microbiote n’arrive pas à capter une variation différente de celle de la variation génétique. Le nombre limité d’animaux étudiés rend difficile une interprétation fine des résultats. Quel que soit le modèle, la prise en compte simultanée du génome et du microbiote n’influe que marginalement sur l’héritabilité des caractères, mais peut conduire à des valeurs de microbiabilité plus faibles que celles obtenues avec un modèle sans l’information génomique. Cela suggère que pour certains caractères, une partie de la variance phénotypique peut être attribuée au microbiote ou au génome, correspondant à des effets indirects de la génétique de l’hôte sur le caractère via les variations du microbiote. Pour tenir compte de cette confusion potentielle entre information microbienne et génomique, Khanal et al. (2020) ont inclus un terme d’interaction génétique × microbiote dans le modèle, afin de séparer les composantes transmissibles et non transmissibles du microbiote. De même, Weishaar et al. (2020) et Christensen et al. (2021) ont proposé des décompositions formelles de la contribution du microbiote à la variance des caractères en composantes génétiques et non génétiques. Les valeurs de microbiabilité dépendent également des choix réalisés pour construire la matrice de relation microbiote, notamment le nombre d’OTU et des méthodes de résolution des équations (Pérez-Enciso et al., 2021).
Les estimations de microbiabilité étant encore peu fréquentes pour les caractères d’intérêt chez le porc, les modélisations proposées dans différentes études peuvent servir de base pour continuer à explorer ce paramètre d’intérêt et estimer l’influence du microbiote en élargissant les caractères étudiés mais aussi les types de microbiotes.
3.3. MiQTL ou MWAS
De même que dans les modèles de prédiction génomique, il est possible de déterminer les effets des marqueurs génétiques utilisés pour construire la matrice de relation génomique, il est possible, à partir des modèles utilisant des matrices de relations basées sur le microbiote, de déterminer les effets significatifs de certains genres sur les caractères prédits, dans une approche « multigenres » (nommées MiQTL ou MWAS). Il s’agit ici de mettre en avant les genres les plus significatifs. En porc, peu d’études ont présenté ce type de résultats (Camarinha-Silva et al., 2017 ; Aliakbari et al., 2022). Dans la première étude (Camarinha-Silva et al., 2017), seuls quelques OTU avaient un effet significatif sur la vitesse de croissance (Uncultured Veillonellaceae, Uncultured Prevotellaceae, Uncultured Proteobacteria), sur l’efficacité alimentaire ou l’ingestion (Uncultured Bacteroidales, Uncultured Clostridiales). Dans la seconde étude (Aliakbari et al., 2022) les genres Streptococcus, Prevotella_9, Ruminococcus_1, Ruminococcaceae_UCG-014, Alloprevotella, XBB1006 (et quelques OTU non associés à un genre bactérien) ont des effets significatifs sur des caractères d’efficacité alimentaire ou d’ingestion. En comparant les résultats obtenus par une régression OTU par OTU ou par une approche multi-OTU, ceux-ci diffèrent peu et mettent en évidence les mêmes genres les plus liés au caractère.
4. La sélection de l’holobionte
Le concept d’holobionte prend tout son sens lorsque l’on considère la coévolution entre le génome de l’hôte et celui de son microbiote. Cette coévolution suggère que l’évolution des populations et de leurs partenaires microbiens est interconnectée et interdépendante.
Il faut envisager que dans certaines conditions de sélection, il serait possible de déterminer les polymorphismes génétiques de l’hôte qui favorisent une meilleure coopération avec des bactéries, par exemple capables de dégrader des fibres alimentaires spécifiques présentes dans leur régime. Ainsi, les gènes de l’hôte et ceux des microorganismes pourraient coévoluer pour optimiser l’utilisation de ressources diversifiées et variables. On pourrait ainsi envisager de favoriser des holobiontes qui s’adaptent plus rapidement aux variations de leur environnement et ainsi améliorer la résilience des populations sélectionnées.
4.1. Prendre en compte le microbiote pour affiner la précision des prédictions
L’un des prérequis de l’amélioration génétique est de pouvoir estimer de la manière la plus précise possible la valeur génétique des candidats à la sélection. Cela peut impliquer de mieux identifier les effets d’environnement agissant sur les caractères ou de trouver des caractères d’intérêt plus héritables. La sélection génétique des individus est fondée sur des modèles de prédiction des valeurs génétiques estimant un effet génétique et des effets d’environnement sur les caractères. Étant donné l’influence du microbiote sur les caractères d’intérêt en production porcine, des modélisations incluant le microbiote comme covariable ont été proposées. L’intérêt d’inclure le microbiote est évalué en comparant la précision de l’estimation des phénotypes incluant le microbiote (à savoir la corrélation entre le phénotype prédit et le phénotype observé), à celle obtenue avec des modélisations classiques (effet génétique et effets d’environnement, sans prendre en compte le microbiote). De manière générale, les résultats disponibles dans la littérature tendent à indiquer un impact positif de la combinaison des données du génotype et du microbiote pour améliorer la précision de la prédiction d’un phénotype (Calle-García et al., 2023). Il existe des modèles partiels incluant uniquement le génotype (modélisation classique) ou uniquement le microbiote (modèle de prédiction microbienne). Leur supériorité par rapport aux modèles traitant l’holobionte dans son ensemble est très variable selon le caractère considéré et dépend du rapport entre la valeur de l’héritabilité et celle de la microbiabilité.
Les modélisations linéaires combinant G (génomique) et M (microbiote) ne sont pas forcément optimales car elles ne tiennent pas compte des interactions possibles entre le génome et le microbiote. Un phénotype de l’hôte peut ainsi être déterminé par son génotype, son microbiote (lui-même influencé par le génotype et par l’environnement). Afin de mieux prendre en compte ces interactions, des modélisations avec des effets récursifs (Christensen et al., 2021) ou des modèles avec des équations structurelles (Tiezzi et al., 2021) ont été développées (figure 3). Cependant, en raison de la complexité de mise en œuvre de ces méthodes et le peu de gain de précision constaté, peu d’études prennent en compte cette interaction.
Pour les caractères d’efficacité alimentaire et de croissance, la précision des prédictions des phénotypes est généralement améliorée quand l’information du microbiote est ajoutée au modèle (Aliakbari et al., 2022 ; Déru et al., 2022b), de même que pour certains caractères de la réponse immunitaire (Calle-García et al., 2023). Pour les caractères de qualité de viande et de composition de la carcasse, l’inclusion de l’information sur le microbiote, caractérisé en fin d’engraissement, améliore la précision de prédiction des phénotypes (Khanal et al., 2020) même en intégrant un terme d’interaction entre l’effet génétique et le microbiote. La prise en compte de l’interaction apporte peu en termes de précision pour la plupart des caractères avec une augmentation de 7,5 % maximum). Cette étude montre entre autres que l’une des limites du modèle de prédiction microbienne est liée au fait que la composition microbienne de l’intestin grêle des porcs n’est pas constante, mais change de la naissance à l’âge adulte, et qu’elle est, bien sûr, affectée par les conditions environnementales. La composition microbienne mesurée à un stade précoce peut ne pas être informative pour prédire des caractères mesurés à un âge plus tardif. De même, les compositions microbiennes prélevées à différents endroits peuvent présenter des capacités différentes de prédiction de caractères complexes.
De plus, avec leur approche, Tiezzi et al. (2021) ont mis en évidence plusieurs variantes génomiques de l’hôte qui affectent des caractères d’adiposité. L’effet du génome de l’hôte est modélisé comme un effet direct, mais aussi comme un effet sur les caractéristiques du microbiote, qui à leur tour affectent le phénotype d'intérêt (figure 3). Dans cette étude, le déterminisme génétique est qualifié par les différences de marqueurs génétiques influençant directement ou indirectement les phénotypes. Démontré au niveau génotypique, on peut supposer que des mécanismes similaires peuvent être mis en évidence pour les caractères sous contrôle polygénique. Sélectionner sur des valeurs génétiques (ou génomiques) estimées avec ce type de modélisation pourrait permettre de prendre en compte de manière optimale le microbiote. Il faut cependant s’assurer d’avoir les données permettant de partitionner correctement les différentes variances.
Le modèle M1 estime l'effet des caractéristiques génomiques de l'hôte sur son phénotype. Le modèle M2 estime l'effet des caractéristiques microbiennes sur le phénotype de l'hôte. Le modèle M4 estime l'effet direct des caractéristiques génomiques de l'hôte sur son phénotype ainsi que leur effet indirect par l'intermédiaire des caractéristiques microbiennes. Le modèle M4L remplace les mesures du phénotype P par une variable latente π qui influence trois phénotypes mesurés (P1, P2, P3).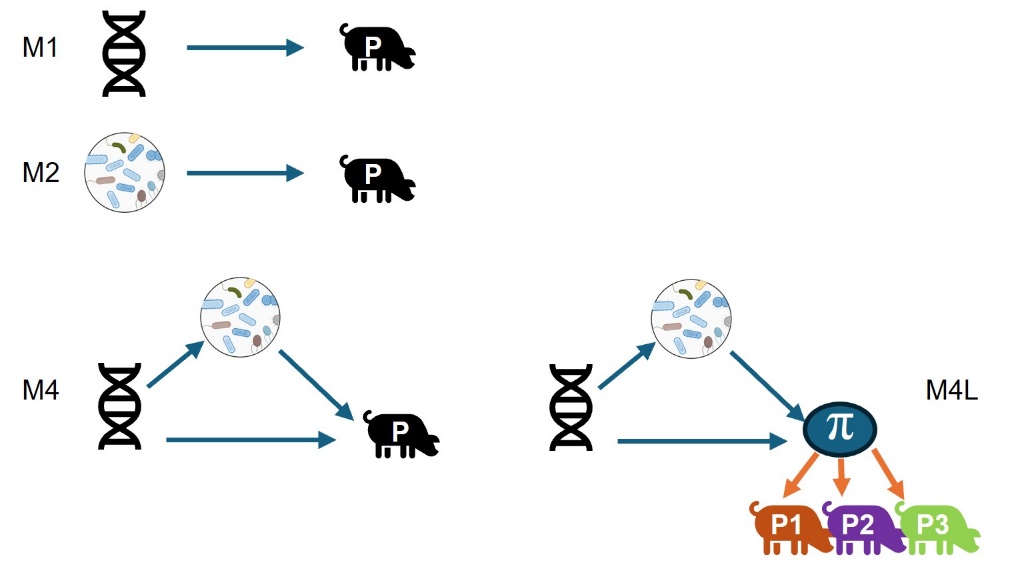
Figure 3. Représentations graphiques des modèles combinant génotype et microbiote pour prédire les caractères de l’hôte, d’après Tiezzi et al. (2021).
Pour l’amélioration génétique, il est plus particulièrement intéressant de connaître l’incidence de la prise en compte du microbiote sur la précision des valeurs génétiques (ou génomiques) mais peu d’études s’y intéressent car en dehors d’observations fondées sur des données simulées, il n’est pas possible de connaître la valeur génétique vraie permettant d’estimer la précision des valeurs génétiques. Christensen et al. (2021) ont montré sur des données simulées qu’un modèle incluant des données « omiques », donc applicable aux données métagénomiques, améliorait la précision des valeurs génomiques. On peut cependant caractériser le reclassement des valeurs génétiques des individus dans les modèles incluant le microbiote par rapport à ceux ne l’incluant pas. Sur des données réelles, en utilisant un modèle incluant conjointement l’effet animal et le microbiote, des reclassements sur les valeurs génétiques de l’efficacité digestive sont possibles, pour des animaux nourris avec un régime fibreux (Déru et al., 2022b).
4.2. La sélection directe sur le microbiote
Une autre manière de prendre en compte le microbiote pour améliorer les caractères de l’hôte est une sélection directe sur les abondances relatives des genres bactériens favorables. Les valeurs d’héritabilité modérées pour un certain nombre de genres bactériens laissent supposer que cette approche est réaliste. Il existe plusieurs difficultés avant de mettre en place ce type de sélection : bien identifier le microbiote d’intérêt et au sein de ce microbiote les genres les plus pertinents, estimer de manière suffisamment précise les paramètres génétiques pour choisir des genres héritables (au sens de l’hôte), et évaluer les conséquences directes et indirectes de la sélection sur les genres.
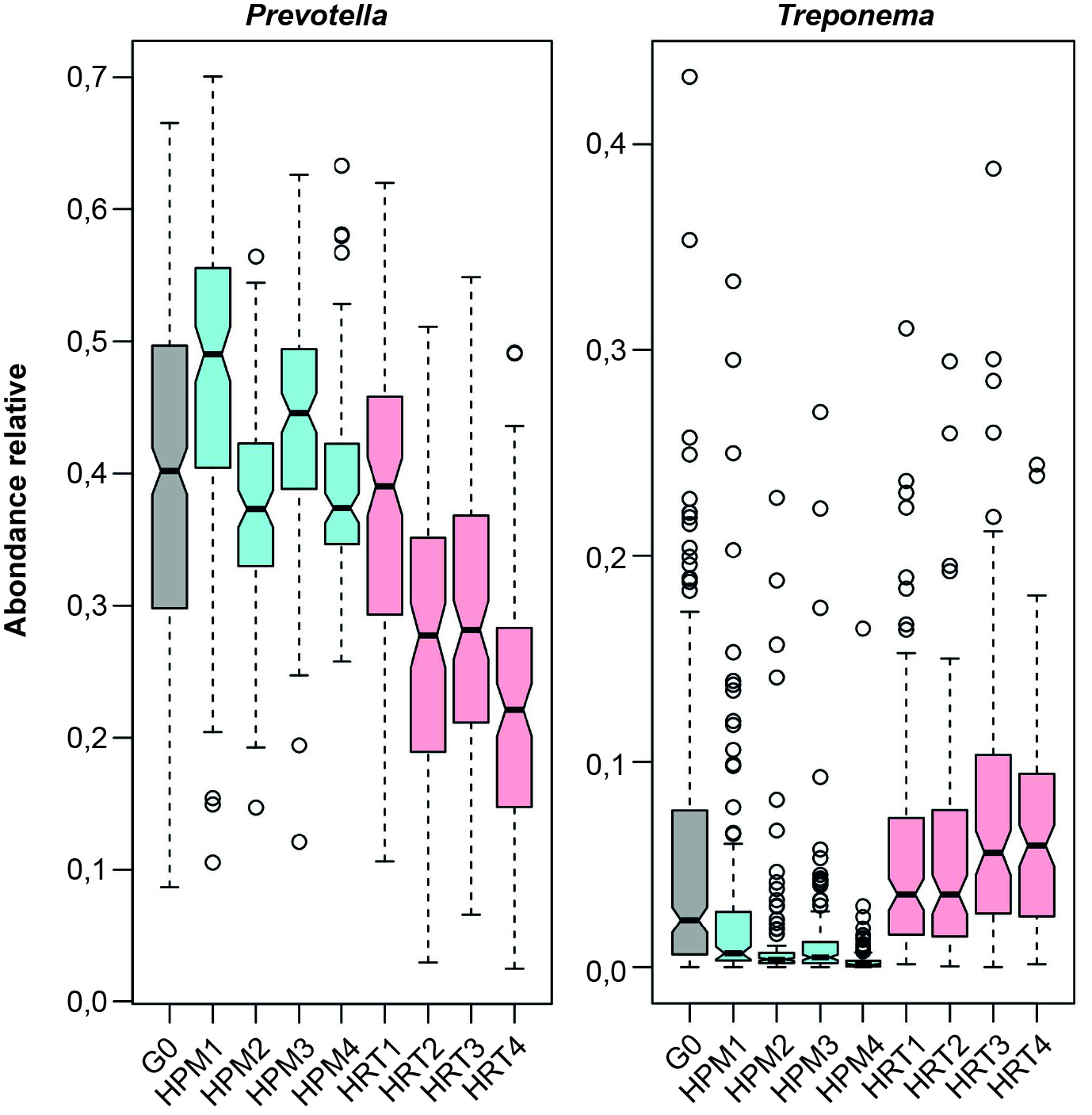
Figure 4. Abondances relatives des genres Prevotella et Treponema dans les lignées porcines sélectionnées pour une augmentation des genres Prevotella et Mitsuokella (HPM, bleu) ou Treponema et Ruminococcus (HRT, rose) dans les générations de sélection de G0 (population de base en gris) à G4.
Une démonstration expérimentale d’une sélection directe sur les abondances relatives de genres bactériens mesurées dans le microbiote fécal de porcs de 60 jours a été réalisée (Larzul et al., 2024). Dans cette expérience, le critère de sélection a été défini sur la base des entérotypes RT/PM et des taxons-clés associés (Ramayo-Caldas et al., 2016). Une lignée a été sélectionnée pour augmenter l’abondance de Prevotella et Mitsuokella (HPM) et l’autre pour augmenter l’abondance relative de Treponema et Ruminococcus (HRT).
La sélection a été efficace, les divergences entre les deux lignées augmentant au fil des générations de sélection (figure 4) avec, dans la lignée HRT, une forte diminution de l’abondance relative de Prevotella et une augmentation de l’abondance relative de Treponema. Dans la lignée HPM, l’abondance relative de Prevotella n’est pas marquée mais au cours de génération, Treponema a progressivement disparu. En regardant les différences sur une échelle standardisée, où chaque unité représente un écart-type du caractère, celles-ci ont atteint une à deux unités d’écart-type à la 4e génération de sélection (Larzul et al., 2025a). Les réponses corrélées ont montré, comme attendu, une amélioration de la croissance post-sevrage dans la lignée sélectionnée sur Prevotella, de l’ordre de +80 g/j à la 4e génération de sélection, par rapport à la lignée HRT.
Conclusion
Chez le porc, les études se sont focalisées sur le microbiote intestinal des animaux en croissance, et son proxy le microbiote fécal, en raison de son implication dans la digestion des aliments et ses liens avec les réponses immunitaires. Le microbiote vaginal a également été étudié du point de vue génétique. Il reste cependant à étendre les études à d’autres microbiotes, notamment nasal qui serait potentiellement d’intérêt en lien avec la santé respiratoire des porcs. Dans une perspective évolutive, la combinaison de plusieurs microbiotes sera nécessaire pour appréhender complètement le concept d’holobionte. Raisonner à cette échelle remet en question la vision traditionnelle de l’évolution basée uniquement sur les gènes de l’hôte. En effet, les interactions symbiotiques avec les microbiotes peuvent influencer le résultat de la sélection. Chez les porcs, certains genres bactériens pourraient conférer des avantages adaptatifs en améliorant la résistance aux maladies ou en augmentant l’efficacité digestive. Le concept d’holobionte ouvre aussi la voie à une meilleure compréhension des relations complexes entre un organisme et ses partenaires microbiens. Ces connaissances devront être mieux prises en compte dans la gestion des populations pour promouvoir des pratiques plus durables et respectueuses de la santé et du bien-être animal. Les modélisations proposées pour la compréhension des rôles directs et indirects du génome de l’hôte et du génome du microbiote sur les phénotypes de l’hôte doivent être plus généralement utilisées sur les données actuellement collectées. Une meilleure description des aspects fonctionnels de l’hôte et des microbiotes par des approches métagénomiques, mais aussi métatranscriptomiques, seront indispensables pour décrire finement les relations hôte/microbiote. À terme, il faudra pouvoir caractériser et prendre en compte la plasticité du microbiote au cours de la vie des individus, sous l’influence de l’évolution de son environnement mais aussi sous contrôle génétique de son hôte. Il ne s’agirait pas de rajouter une information sur le microbiote a un instant donné, choisi sur la base de ses relations avec les phénotypes d’intérêt, mais de considérer aussi le potentiel d’évolution du microbiote en lien avec les modifications observées ou possibles de son environnement. Développer des approches longitudinales apportera les connaissances nécessaires à cette dimension évolutive au cours de la vie, propice à l’adaptation.
Remerciements
La rédaction de cette synthèse a bénéficié des réflexions sur le déterminisme génétique du microbiote, menées dans le cadre du réseau Holo-AE financé par le métaprogramme INRAE Holoflux.
Notes
- 1. Cette publication a fait l’objet d’une première publication et présentation lors des 57e Journées de la Recherche Porcine (Larzul et al., 2025b).
Références
- Aliakbari, A., Zemb, O., Billon, Y., Barilly, C., Ahn, I., Riquet, J., & Gilbert, H. (2021). Genetic relationships between feed efficiency and gut microbiome in pig lines selected for residual feed intake. Journal of Animal Breeding and Genetics, 138(4), 491-507. https://doi.org/10.1111/jbg.12539
- Aliakbari, A., Zemb, O., Cauquil, L., Barilly, C., Billon, Y., & Gilbert, H. (2022). Microbiability and microbiome-wide association analyses of feed efficiency and performance traits in pigs. Genetics Selection Evolution, 54(1), 29. https://doi.org/10.1186/s12711-022-00717-7
- Arumugam, M., Raes, J., Pelletier, E., Le Paslier, D., Yamada, T., Mende, D. R., Fernandes, G. R., Tap, J., Bruls, T., Batto, J.-M., Bertalan, M., Borruel, N., Casellas, F., Fernandez, L., Gautier, L., Hansen, T., Hattori, M., Hayashi, T., … Bork, P. (2011). Enterotypes of the human gut microbiome. Nature, 473, 174-180. https://doi.org/10.1038/nature09944
- Bergamaschi, M., Maltecca, C., Schillebeeckx, C., McNulty, N. P., Schwab, C., Shull, C., Fix, J., & Tiezzi, F. (2020a). Heritability and genome-wide association of swine gut microbiome features with growth and fatness parameters. Scientific Reports, 10, 10134. https://doi.org/10.1038/s41598-020-66791-3
- Bergamaschi, M., Tiezzi, F., Howard, J., Huang, Y. J., Gray, K. A., Schillebeeckx, C., McNulty, N. P., & Maltecca, C. (2020b). Gut microbiome composition differences among breeds impact feed efficiency in swine. Microbiome, 8, 110. https://doi.org/10.1186/s40168-020-00888-9
- Bergman, E. N. (1990). Energy contributions of volatile fatty acids from the gastrointestinal tract in various species. Physiological Reviews, 70(2), 567-590. https://doi.org/10.1152/physrev.1990.70.2.567
- Borey, M., Estellé, J., & Rogel-Gaillard, C. (2022). Understanding the development of the gut microbiome in pigs: an overview. In M. Bailey M. & C. Stokes (Eds.), Understanding gut microbiomes as targets for improving pig gut health (pp. 179-202), Burleigh Dodds Science Publishing. https://dx.doi.org/10.19103/AS.2021.0089.07
- Calle-García, J., Ramayo-Caldas, Y., Zingaretti, L. M., Quintanilla, R., Ballester, M., & Pérez-Enciso, M. (2023). On the holobiont ‘predictome’ of immunocompetence in pigs. Genetics Selection Evolution, 55, 29. https://doi.org/10.1186/s12711-023-00803-4
- Camarinha-Silva, A., Maushammer, M., Wellmann, R., Vital, M., Preuss, S., & Bennewitz, J. (2017). Host genome influence on gut microbial composition and microbial prediction of complex traits in pigs. Genetics, 206(3), 1637-1644. https://doi.org/10.1534/genetics.117.200782
- Chen, C., Huang, X., Fang, S., Yang, H., He, M., Zhao, Y., & Huang, L. (2018). Contribution of host genetics to the variation of microbial composition of cecum lumen and feces in pigs. Frontiers in Microbiology, 9, 2626. https://doi.org/10.3389/fmicb.2018.02626
- Chen, C., Zhou, Y., Fu, H., Xiong, X., Fang, S., Jiang, H., Wu, J., Yang, H., Gao, J., & Huang, L. (2021). Expanded catalog of microbial genes and metagenome-assembled genomes from the pig gut microbiome. Nature Communications, 12, 1106. https://doi.org/10.1038/s41467-021-21295-0
- Christensen, O. F., Börner, V., Varona, L., & Legarra, A. (2021). Genetic evaluation including intermediate omics features. Genetics, 219(2), iyab130. https://doi.org/10.1093/genetics/iyab130
- Crespo-Piazuelo, D., Migura-Garcia, L., Estellé, J., Criado-Mesas, L., Revilla, M., Castelló, A., Muñoz, M., García-Casco, J. M., Fernández, A. I., Ballester, M., & Folch, J. M. (2019). Association between the pig genome and its gut microbiota composition. Scientific Reports, 9, 8791. https://doi.org/10.1038/s41598-019-45066-6
- David, I., & Ricard, A. (2019). A unified model for inclusive inheritance in livestock species. Genetics, 212(4), 1075-1099. https://doi.org/10.1534/genetics.119.302375
- Déru, V., Bouquet, A., Zemb, O., Blanchet, B., De Almeida, M. L., Cauquil, L., Carillier-Jacquin, C., & Gilbert, H. (2022a). Genetic relationships between efficiency traits and gut microbiota traits in growing pigs being fed with a conventional or a high-fiber diet. Journal of Animal Science, 100(6), skac183. https://doi.org/10.1093/jas/skac183
- Déru, V., Tiezzi, F., Carillier-Jacquin, C., Blanchet, B., Cauquil, L., Zemb, O., Bouquet, A., Maltecca, C., & Gilbert, H. (2022b). Gut microbiota and host genetics contribute to the phenotypic variation of digestive and feed efficiency traits in growing pigs fed a conventional and a high fiber diet. Genetics Selection Evolution, 54(1), 55. https://doi.org/10.1186/s12711-022-00742-6
- Difford, G. F., Lassen, J., & Løvendahl, P. (2016). Genes and microbes, the next step in dairy cattle breeding [Communication]. 67th Annual Meeting of the European Federation of Animal Science, Belfast. https://docs.eaap.org/boa/2016_Belfast_EAAP_Book_Abstracts.pdf
- Federhen, S. (2012). The NCBI Taxonomy database. Nucleic Acids Research, 40, D136-D143. https://doi.org/10.1093/nar/gkr1178
- Flint, H. J., Bayer, E. A., Rincon, M. T., Lamed, R., & White, B. A. (2008). Polysaccharide utilization by gut bacteria: potential for new insights from genomic analysis. Nature Reviews Microbiology, 6(2), 121-131. https://doi.org/10.1038/nrmicro1817
- Frioux, C., Ansorge, R., Özkurt, E., Ghassemi Nedjad, C., Fritscher, J., Quince, C., Waszak, S. M., & Hildebrand, F. (2023). Enterosignatures define common bacterial guilds in the human gut microbiome. Cell Host & Microbe, 31(7), 1111-1125.e6. https://doi.org/10.1016/j.chom.2023.05.024
- Haegeman, B., Hamelin, J., Moriarty, J., Neal, P., Dushoff, J., & Weitz, J. S. (2013). Robust estimation of microbial diversity in theory and in practice. The ISME Journal, 7(6), 1092-1101. https://doi.org/10.1038/ismej.2013.10
- He, Y., Tiezzi, F., Howard, J., Huang, Y., Gray, K., & Maltecca, C. (2022). Exploring the role of gut microbiota in host feeding behavior among breeds in swine. BMC Microbiology, 22, 1. https://doi.org/10.1186/s12866-021-02409-6
- Huang, L., & Chen, C. (2023). Employing pigs to decipher the host genetic effect on gut microbiome: advantages, challenges, and perspectives. Gut Microbes, 15(1), 2205410. https://doi.org/10.1080/19490976.2023.2205410
- Ke, S., Fang, S., He, M., Huang, X., Yang, H., Yang, B., Chen, C., & Huang, L. (2019). Age-based dynamic changes of phylogenetic composition and interaction networks of health pig gut microbiome feeding in a uniformed condition. BMC Veterinary Research, 15, 172. https://doi.org/10.1186/s12917-019-1918-5
- Khanal, P., Maltecca, C., Schwab, C., Fix, J., Bergamaschi, M., & Tiezzi, F. (2020). Modeling host-microbiome interactions for the prediction of meat quality and carcass composition traits in swine. Genetics Selection Evolution, 52, 41. https://doi.org/10.1186/s12711-020-00561-7
- Khanal, P., Maltecca, C., Schwab, C., Fix, J., & Tiezzi, F. (2021). Microbiability of meat quality and carcass composition traits in swine. Journal of Animal Breeding and Genetics, 138(2), 223-236. https://doi.org/10.1111/jbg.12504
- Kubasova, T., Davidova-Gerzova, L., Babak, V., Cejkova, D., Montagne, L., Le-Floc’h, N., & Rychlik, I. (2018). Effects of host genetics and environmental conditions on fecal microbiota composition of pigs. Plos One, 13(8), e0201901. https://doi.org/10.1371/journal.pone.0201901
- Larzul, C., Blanc, F., Lemonnier, G., Jardet, D., Niort, C., Rogel-Gaillard, C., & Estellé, J. (2025a). La sélection de l’hôte est efficace pour orienter le microbiote intestinal chez le porc [Communication]. 57e Journées de la Recherche Porcine, Saint-Malo. https://www.journees-recherche-porcine.com/texte/2025/genetique/g01.pdf
- Larzul, C., Estellé, J., Borey, M., Blanc, F., Lemonnier, G., Billon, Y., Thiam, M. G., Quinquis, B., Galleron, N., Jardet, D., Lecardonnel, J., Plaza Oñate, F., & Rogel-Gaillard, C. (2024). Driving gut microbiota enterotypes through host genetics. Microbiome, 12, 116. https://doi.org/10.1186/s40168-024-01827-8
- Larzul, C., Rogel-Gaillard, C., Carillier-Jacquin, C., Déru V., & Estelle, J. (2025b). L’holobionte, une nouvelle dimension pour la sélection porcine ? [Communication]. 57e Journées Recherche Porcine, Saint-Malo. https://www.journees-recherche-porcine.com/texte/2025/genetique/g02.pdf
- Ley, R. E., Lozupone, C. A., Hamady, M., Knight, R., & Gordon, J. I. (2008). Worlds within worlds: evolution of the vertebrate gut microbiota. Nature Reviews Microbiology, 6, 776-788. https://doi.org/10.1038/nrmicro1978
- Ley, R. E., Turnbaugh, P. J., Klein, S., & Gordon, J. I. (2006). Human gut microbes associated with obesity. Nature, 444, 1022-1023. https://doi.org/10.1038/4441022a
- Lin, H., & Peddada, S. D. (2020). Analysis of microbial compositions: a review of normalization and differential abundance analysis. Npj Biofilms and Microbiomes, 6, 60. https://doi.org/10.1038/s41522-020-00160-w
- Lu, D., Tiezzi, F., Schillebeeckx, C., McNulty, N. P., Schwab, C., Shull, C., & Maltecca, C. (2018). Host contributes to longitudinal diversity of fecal microbiota in swine selected for lean growth. Microbiome, 6, 4. https://doi.org/10.1186/s40168-017-0384-1
- Luise, D., Le Sciellour, M., Buchet, A., Resmond, R., Clément, C., Rossignol, M.-N., Jardet, D., Zemb, O., Belloc, C., & Merlot, E. (2021). The fecal microbiota of piglets during weaning transition and its association with piglet growth across various farm environments. PLoS ONE, 16(4), e0250655. https://doi.org/10.1371/journal.pone.0250655
- Luo, Z.-B., Han, S., Yin, X.-J., Liu, H., Wang, J., Xuan, M., Hao, C., Wang, D., Liu, Y., Chang, S., Li, D., Gao, K., Li, H., Quan, B., Quan, L.-H., & Kang, J.-D. (2023). Fecal transplant from myostatin deletion pigs positively impacts the gut-muscle axis. Elife, 12, e81858. https://doi.org/10.7554/eLife.81858
- Mach, N., Berri, M., Estellé, J., Levenez, F., Lemonnier, G., Denis, C., Leplat, J.-J, Chevaleyre, C., Billon, Y., Doré, J., Rogel‐Gaillard, C., & Lepage, P. (2015). Early‐life establishment of the swine gut microbiome and impact on host phenotypes. Environmental Microbiology Reports, 7(3), 554-569. https://doi.org/10.1111/1758-2229.12285
- Maltecca, C., Bergamaschi, M., & Tiezzi, F. (2020). The interaction between microbiome and pig efficiency: A review. Journal of Animal Breeding and Genetics, 137, 4-13. https://doi.org/10.1111/jbg.12443
- Martens, E. C., Lowe, E. C., Chiang, H., Pudlo, N. A., Wu, M., McNulty, N. P., Abbott, D. W., Henrissat, B., Gilbert, H. J., Bolam, D. N., & Gordon, J. I. (2011). Recognition and degradation of plant cell wall polysaccharides by two human gut symbionts. PLoS Biology, 9(12), e1001221. https://doi.org/10.1371/journal.pbio.1001221
- McDonald, D., Jiang, Y., Balaban, M., Cantrell, K., Zhu, Q., Gonzalez, A., Morton, J. T., Nicolaou, G., Parks, D. H., Karst, S. M., Albertsen, M., Hugenholtz, P., DeSantis, T., Song, S. J., Bartko, A., Havulinna, A. S., Jousilahti, P., Cheng, S., Inouye, M., … Knight, R. (2024). Greengenes2 unifies microbial data in a single reference tree. Nature Biotechnology, 42(5), 715-718. https://doi.org/10.1038/s41587-023-01845-1
- Pérez-Enciso, M., Zingaretti, L. M., Ramayo-Caldas, Y., & De Los Campos, G. (2021). Opportunities and limits of combining microbiome and genome data for complex trait prediction. Genetics Selection Evolution, 53, 65. https://doi.org/10.1186/s12711-021-00658-7
- Plaza Oñate, F., Ghozlane, A., & Almeida, M. (2021). An updated catalog of genes and species of the pig gut microbiota [Data set]. Data INRAE. https://doi.org/10.15454/OPAULL
- Quast, C., Pruesse, E., Yilmaz, P., Gerken, J., Schweer, T., Yarza, P., Peplies, J., & Glöckner, F. O. (2012). The SILVA ribosomal RNA gene database project: improved data processing and web-based tools. Nucleic Acids Research, 41, D590-D596. https://doi.org/10.1093/nar/gks1219
- Ramayo-Caldas, Y., Mach, N., Lepage, P., Levenez, F., Denis, C., Lemonnier, G., Leplat, J.-J., Billon, Y., Berri, M., Doré, J., Rogel-Gaillard, C., & Estellé, J. (2016). Phylogenetic network analysis applied to pig gut microbiota identifies an ecosystem structure linked with growth traits. The ISME Journal, 10(12), 2973-2977. https://doi.org/10.1038/ismej.2016.77
- Ramayo-Caldas, Y., Prenafeta-Boldú, F., Zingaretti, L. M., Gonzalez-Rodriguez, O., Dalmau, A., Quintanilla, R., & Ballester, M. (2020). Gut eukaryotic communities in pigs: diversity, composition and host genetics contribution. Animal Microbiome, 2, 18. https://doi.org/10.1186/s42523-020-00038-4
- Ramayo-Caldas, Y., Zingaretti, L. M., Pérez-Pascual, D., Alexandre, P. A., Reverter, A., Dalmau, A., Quintanilla, R., & Ballester, M. (2021). Leveraging host-genetics and gut microbiota to determine immunocompetence in pigs. Animal Microbiome, 3, 74. https://doi.org/10.1186/s42523-021-00138-9
- Reverter, A., Ballester, M., Alexandre, P. A., Mármol-Sánchez, E., Dalmau, A., Quintanilla, R., & Ramayo-Caldas, Y. (2021). A gene co-association network regulating gut microbial communities in a Duroc pig population. Microbiome, 9, 52. https://doi.org/10.1186/s40168-020-00994-8
- Rosenberg, E., & Zilber-Rosenberg, I. (2018). The hologenome concept of evolution after 10 years. Microbiome, 6, 78. https://doi.org/10.1186/s40168-018-0457-9
- Sanglard, L. P., Schmitz‐Esser, S., Gray, K. A., Linhares, D. C. L., Yeoman, C. J., Dekkers, J. C. M., Niederwerder, M. C., & Serão, N. V. L. (2020). Investigating the relationship between vaginal microbiota and host genetics and their impact on immune response and farrowing traits in commercial gilts. Journal of Animal Breeding and Genetics, 137, 84-102. https://doi.org/10.1111/jbg.12456
- Tancredi, A., Matthijs, T., Cox, E., Van Immerseel, F., & Goossens, E. (2025). From mother to piglet: the lasting influence of the maternal microbiome. Animal Microbiome, 7, 52. https://doi.org/10.1186/s42523-025-00420-0
- Tiezzi, F., Fix, J., Schwab, C., Shull, C., & Maltecca, C. (2021). Gut microbiome mediates host genomic effects on phenotypes: a case study with fat deposition in pigs. Computational and Structural Biotechnology Journal, 19, 530-544. https://doi.org/10.1016/j.csbj.2020.12.038
- Verschuren, L. M. G., Schokker, D., Bergsma, R., Jansman, A. J. M., Molist, F., & Calus, M. P. L. (2020). Prediction of nutrient digestibility in grower‐finisher pigs based on faecal microbiota composition. Journal of Animal Breeding and Genetics, 137, 23-35. https://doi.org/10.1111/jbg.12433
- Vourlaki, I.-T., Rio-Lopez, R., Clavell-Sansalvador, A., Ramírez-Ayala, L. C., Ballester, M., Sanchez, J. P., Piles, M., Quintanilla, R., Da Fonseca de Oliveira, A. C., Costa, L. B., Dalmau, A., & Ramayo-Caldas, Y. (2025). Co-occurring microbial guilds in pig fecal microbiota: key drivers and effects on host performance. Genetics Selection Evolution, 57, 27. https://doi.org/10.1186/s12711-025-00979-x
- Walker, A. W., & Hoyles, L. (2023). Human microbiome myths and misconceptions. Nature Microbiology, 8, 1392-1396. https://doi.org/10.1038/s41564-023-01426-7
- Wang, Q., Garrity, G. M., Tiedje, J. M., & Cole, J. R. (2007). Naïve bayesian classifier for rapid assignment of rRNA sequences into the new bacterial taxonomy. Applied and Environmental Microbiology, 73(16), 5261-5267. https://doi.org/10.1128/AEM.00062-07
- Wang, X., Tsai, T., Deng, F., Wei, X., Chai, J., Knapp, J., Apple, J., Maxwell, C. V., Lee, J. A., Li, Y., & Zhao, J. (2019). Longitudinal investigation of the swine gut microbiome from birth to market reveals stage and growth performance associated bacteria. Microbiome, 7, 109. https://doi.org/10.1186/s40168-019-0721-7
- Weishaar, R., Wellmann, R., Camarinha‐Silva, A., Rodehutscord, M., & Bennewitz, J. (2020). Selecting the hologenome to breed for an improved feed efficiency in pigs—A novel selection index. Journal of Animal Breeding and Genetics, 137, 14-22. https://doi.org/10.1111/jbg.12447
- Xiao, L., Estellé, J., Kiilerich, P., Ramayo-Caldas, Y., Xia, Z., Feng, Q., Liang, S., Pedersen, A. Ø., Kjeldsen, N. J., Liu, C., Maguin, E., Doré, J., Pons, N., Le Chatelier, E., Prifti, E., Li, J., Jia, H., Liu, X., Xu, X., … Wang, J. (2016). A reference gene catalogue of the pig gut microbiome. Nature Microbiology, 1, 16161. https://doi.org/10.1038/nmicrobiol.2016.161
- Yang, H., Wu, J., Huang, X., Zhou, Y., Zhang, Y., Liu, M., Liu, Q., Ke, S., He, M., Fu, H., Fang, S., Xiong, X., Jiang, H., Chen, Z., Wu, Z., Gong, H., Tong, X., Huang, Y., Ma, J., … Huang, L. (2022). ABO genotype alters the gut microbiota by regulating GalNAc levels in pigs. Nature, 606, 358-367. https://doi.org/10.1038/s41586-022-04769-z
- Zemb, O., Achard, C. S., Hamelin, J., De Almeida, M.-L., Gabinaud, B., Cauquil, L., Verschuren, L. M. G., & Godon, J.-J. (2020). Absolute quantitation of microbes using 16S rRNA gene metabarcoding: A rapid normalization of relative abundances by quantitative PCR targeting a 16S rRNA gene spike-in standard. MicrobiologyOpen, 9(3), e977. https://doi.org/10.1002/mbo3.977
Résumé
Le rôle du microbiote et en particulier du microbiote intestinal sur les performances de l’hôte est de plus en plus documenté chez les animaux d’élevage. Ces avancées ont été permises par l’utilisation des nouvelles techniques de séquençage à haut débit et le développement de méthodes d’analyse des données pour caractériser les microorganismes présents (diversité, abondances relatives, assemblage en écosystèmes). Elles ont apporté de nouvelles connaissances sur les liens entre la diversité génétique de l’hôte et les interactions hôte-microbiote, mais aussi sur l’estimation des phénotypes ou des valeurs génétiques en prenant en compte la variabilité du microbiote. Ces résultats alimentent un nouveau paradigme fondé sur la définition de l’holobionte en tant que système biologique qui assemble un hôte et son microbiote, offrant une nouvelle vision de ce que représente un individu. Nous proposons de faire le point sur l’holobionte porc, en termes de modélisation et de résultats expérimentaux pour comprendre, prédire et piloter les phénotypes dans le but d’améliorer par exemple la santé mais aussi l’efficience productive et environnementale des animaux. Ces avancées sont également discutées comme ouvrant la voie pour élaborer des stratégies de sélection prenant simultanément en compte les informations sur l’hôte et son microbiote en raisonnant l’amélioration durable des populations à l’échelle non plus de l’individu mais de l’holobionte.
Pièces jointes
Pas de document complémentaire pour cet articleStatistiques de l'article
 Vues: 1000
Vues: 1000
Téléchargements
 PDF: 126
PDF: 126
 XML: 35
XML: 35
Articles les plus lus par le même auteur ou la même autrice
- Séverine PAROIS, Michel BONNEAU, Patrick CHEVILLON, Catherine LARZUL, Nathalie QUINIOU, Annie ROBIC, Armelle PRUNIER, Odeurs indésirables de la viande de porcs mâles non castrés : problèmes et solutions potentielles , INRAE Productions Animales: Vol. 31 No 1 (2018)
- Jean-Louis PEYRAUD, Joël AUBIN, Marc BARBIER, René BAUMONT, Cécile BERRI, Jean-Pierre BIDANEL, Christine CITTI, Corinne COTINOT, Christian DUCROT, Pierre DUPRAZ, Philippe FAVERDIN, Nicolas FRIGGENS, Sabine HOUOT, Marie-Odile NOZIÈRES-PETIT, Claire ROGEL-GAILLARD, Véronique SANTÉ-LHOUTELLIER, Quelle science pour les élevages de demain ? Une réflexion prospective conduite à l’INRA , INRAE Productions Animales: Vol. 32 No 2 (2019): Volume 32 Numéro 2 : Numéro spécial. De grands défis et des solutions pour l'élevage
- Jean-Pierre BIDANEL, Parsaoran SILALAHI, Thierry TRIBOUT, Laurianne CANARIO, Alain DUCOS, Hervé GARREAU, Hélène GILBERT, Catherine LARZUL, Denis MILAN, Juliette RIQUET, Sandrine SCHWOB, Marie-José MERCAT, Claire HASSENFRATZ, Alain BOUQUET, Christophe BAZIN, Joel BIDANEL, Cinquante années d’amélioration génétique du porc en France : bilan et perspectives , INRAE Productions Animales: Vol. 33 No 1 (2020)
- Lucile MONTAGNE, Laurent ALIBERT, Cécile BONNEFONT, Jean-Philippe CHOISIS, Amandine DURPOIX, Hélène GILBERT, Souhil HARCHAOUI, Catherine LARZUL, Bénédicte LEBRET, Sarah LOMBARD, Gilles MARTEL, Marc MORAINE, Laurent PICGIRARD, Thomas PUECH, Justine FAURE, Quels défis au développement de la production porcine en agriculture biologique en France ? , INRAE Productions Animales: Vol. 37 No 2 (2024): Numéro spécial : L’élevage biologique : conditions et potentiel de développement
- Laurianne CANARIO, Nicolas BÉDÈRE, Marc VANDEPUTTE, Didier BOICHARD, Jérôme RAOUL, Catherine LARZUL, Quelles génétiques pour les systèmes d’élevages certifiés en agriculture biologique ? , INRAE Productions Animales: Vol. 37 No 2 (2024): Numéro spécial : L’élevage biologique : conditions et potentiel de développement
- Laurianne CANARIO, Catherine LARZUL, La morsure de queue chez le porc : de la mesure aux solutions génétiques pour limiter le phénomène , INRAE Productions Animales: Vol. 38 No 3 (2025)
- Céline CARILLIER-JACQUIN, Hélène LARROQUE, Christèle ROBERT-GRANIÉ, Vers une sélection génomique chez les caprins laitiers , INRAE Productions Animales: Vol. 30 No 1 (2017)

