Le point sur la lipolyse du lait de vache : facteurs de variation et mécanismes biochimiques
Chapeau
La lipolyse du lait est une réaction d’hydrolyse de la matière grasse qui peut être à l’origine de défauts de qualité organoleptique et technologique des laits et des produits laitiers. Les niveaux de lipolyse dépendent de l’animal, des facteurs d’élevage, du matériel de traite et de la présence éventuelle de bactéries psychrotrophes. Ils ne peuvent pas être corrigés par l’industrie laitière, ce qui a motivé de nombreux travaux en amont de la filière, allant de la zootechnie à la biochimie des laits.
Introduction
La lipolyse du lait, un des processus de dégradation de la Matière Grasse (MG) laitière, est un critère de qualité du lait. En effet, les acides gras à chaîne courte libérés lors de la lipolyse provoquent le développement d'un arôme de rance dans le lait, qui n’est pas toléré par les consommateurs Français. De plus, la présence de triglycérides partiels dans le lait nuit à ses propriétés technologiques, telles que ses capacités de moussage et de crémage.
La mesure de la lipolyse s’effectue par dosage des Acides Gras Libres (AGL) des laits, produits de la réaction de lipolyse (cf. encadré). La méthode de dosage la plus utilisée est la méthode des savons de cuivre ; il s’agit d’une méthode colorimétrique étalonnée sur l’acide oléique. L’unité de mesure de lipolyse est le milliéquivalent (meq) pour 100 g de MG qui équivaut à 0,28 g d’acide oléique pour 100 g de MG. Le lait de référence doit contenir moins de 0,89 meq d’AGL pour 100 g de MG. Entre les années 1960 et 1990, l'incidence de la lipolyse du lait a considérablement augmenté en raison de l'intensification de la production laitière (plus de lait produit par vache) et de la modernisation de la traite (machines à traire). À cette époque, d’énormes efforts de recherche et développement ont été déployés pour trouver des stratégies visant à réduire la lipolyse du lait. Cependant, depuis les années 2000, les industries laitières ont à nouveau connu une augmentation des phénomènes de lipolyse dans la collecte du lait en France, sans que cette augmentation soit jusqu'ici objectivée ou expliquée par les techniciens d'élevage. De plus, l’arrivée des robots de traite a entraîné une augmentation de 20 à 50 % des taux de lipolyse par rapport aux installations de traite conventionnelle et des problèmes liés à la lipolyse pourraient apparaître dans les années à venir.
Encadré. Méthodes de mesure de la lipolyse du lait (d’après une plaquette distribuée par le CNIEL : La lipolyse du lait. Comment améliorer ses résultats).
Depuis 2012, pour mesurer l’indice de lipolyse du lait, les laboratoires interprofessionnels laitiers et les CRIEL ont le choix entre deux méthodes de routine validées et autorisées par le CNIEL :
i) Une technique chimique dite « méthode aux savons de cuivre » : cette méthode détermine par réaction colorimétrique les acides gras libres extraits du lait par un solvant organique. Elle consiste en un transfert sélectif des acides gras libres sous forme de savons de cuivre, vers une phase organique à base de chloroforme que l’on sépare du lait. La teneur en savons de cuivre est ensuite déterminée par analyse colorimétrique du cuivre associé aux acides gras libres.
ii) une méthode instrumentale par spectrométrie infrarouge.
Il existe une 3ème méthode qui est la méthode de référence : méthode BDI (ISO/TS 22113 ; FIL/MR204). Une quantité d'échantillon est mélangée soigneusement avec une solution contenant du tétraphosphate de sodium et un agent tensioactif. Le mélange est chauffé dans un bain d'eau bouillante pour obtenir la séparation de la matière grasse. Une quantité connue de matière grasse extraite est dissoute dans un solvant organique et titrée avec un alcali alcoolique.
Les modalités de paiement du lait ont évolué en 2012. D’un contrôle par mois ou par trimestre (selon les régions) avec la méthode aux savons de cuivre, la périodicité est passée à 3 analyses minimum par mois et par producteur (comme pour la matière grasse) avec la méthode infrarouge. Le passage à l’infrarouge permet ainsi d’augmenter la fréquence des analyses. La méthode infrarouge a également l’avantage de délivrer des résultats presque instantanément, d’éviter la manipulation de solvants et de réduire la production de déchets polluants. Il est à noter que le seuil de pénalité reste le même quelle que soit la méthode. Les principes appliqués pour les règles de gestion des écarts (rattrapages) sont maintenus. Le tableau suivant résume les modalités de paiement du lait de vache pour chacune des méthodes d’analyses utilisables, applicables depuis 2012.
* plage de validité des résultats analytiques ** à partir de 2013 unités : milliéquivalent d’acides gras libres par 100 g de matière grasse
On distingue trois types de lipolyse (figure 1) : la Lipolyse Spontanée (LS), la Lipolyse Induite (LI) et la Lipolyse Microbienne (LM). La LS se produit consécutivement au refroidissement du lait, en l’absence de chocs mécaniques. Elle dépend de l’animal et des facteurs d’élevage. La LI se produit consécutivement aux chocs mécaniques et thermiques qui ont lieu pendant la traite et le stockage du lait. En pratique, dans les élevages, il n’est pas possible de dissocier la LS de la LI dans les laits de tank. La LM est le produit de l’action des enzymes microbiennes sur les globules gras du lait. La LM devient significative après 3 à 4 jours de stockage du lait cru, lorsqu’il est de qualité sanitaire satisfaisante.
Figure 1. Les différents types de lipolyse : spontanée, induite et microbienne (d’après Heuchel et Chilliard, 1988).

Cet article de synthèse fait état des connaissances actuelles sur les lipolyses du lait de vache (LS et LI), depuis l’impact sur le lait et les produits laitiers jusqu’aux mécanismes biochimiques. L’impact des facteurs d’élevage et de l’installation de traite est traité avec attention. La LM ne sera pas abordée.
1. Effets sur la qualité organoleptique et technologique du lait et des produits laitiers
1.1. Effet sur la qualité gustative des produits laitiers
L’hydrolyse des TriGlycérides (TG) en AGL par la LipoProtéine Lipase (LPL) peut être à l’origine de modifications organoleptiques des produits laitiers. La contribution des AGL au goût des produits peut être positive ou négative selon les produits considérés. Les seuils de perceptions de ces modifications organoleptiques sont variables en fonction des produits et des jurys de dégustations.
a. Laits liquides, crèmes et beurres
Historiquement, le terme « rance » a été le plus utilisé pour décrire le défaut de goût associé à la lipolyse. Les termes de « savonneux », « chèvre », « butyrique » et « amer » ont également été utilisés. Cependant, les termes « amer » et « rance » ne sont pas spécifiques à la lipolyse et sont parfois utilisés pour décrire des saveurs liées à l’oxydation ou à la dégradation protéique. De ce fait, il est recommandé d’utiliser le terme de « lipolysé » pour faire référence à la saveur spécifique qui correspond à l’hydrolyse des TG (Shipe et al., 1978). Cependant cette nomenclature n’est pas toujours respectée dans la littérature et le terme de « rance » est souvent rencontré (Scanlan et al., 1965 ; Duncan et al., 1991 ; Gonzalez-Cordova et Vallejo-Cordoba, 2003). Il a été montré que la flaveur « lipolysée » du lait provenait essentiellement des acides gras à courte chaîne (C4:0 à C12:0) et particulièrement de l’acide caprylique (C8:0) et de l’acide caprique (C10:0) (tableau 1 ; Scanlan et al., 1965 ; Bendall, 2001 ; Moio et al., 1993). Dans le beurre, la présence d’AGL perturbe l’équilibre entre composés volatiles et non-volatiles en apportant une saveur et une odeur « rances » aux beurres (tableau 2 ; Shipe et al., 1980 ; Gonzalez-Cordova et Vallejo-Cordoba, 2003 ; Mallia et al., 2008). L’acide butyrique (C4:0) et l’acide caproïque (C6:0) seraient les AGL les plus influents (McDaniel et al., 1969). Concernant les yaourts, il y a peu d’information dans la littérature. Cependant, il a été montré une corrélation positive entre une saveur de type « savon » dans les yaourts et la concentration en AGL, et plus particulièrement en C8:0, C10:0 et C14:0 (Cheng, 2010).
Tableau 1. Flaveurs associées aux acides gras libres à courte chaîne présents dans le lait des vaches laitières (adapté de Chouinard et al., 2012 ; Bendall, 2001 ; Moio et al., 1993).
Acide gras |
Flaveur associée |
|---|---|
Acide acétique |
Vinaigre |
Acide propionique |
Vinaigre ; âcre |
Acide butyrique |
Vomi ; fromage féta |
Acide valérique |
Acide ; pain ; fromage ; chien |
Acide caproïque |
Graisseux ; fromageux ; cireux ; chèvre |
Acide caprylique |
Cire ; savon ; chèvre ; moisi ; rance ; fruité |
Acide caprique |
Rance |
Acide déc-9-énoique |
Papier humide ; poussière brûlée |
Acide 3-méthylbutanoïque |
Herbeux léger ; légumes cuits |
Tableau 2. Acides gras libres à courte chaîne participant à l’odeur des beurres (adapté de Mallia et al., 2008).
Composant |
Odeur associée |
Seuil odeur nasale (mg/kg) |
|---|---|---|
Acide butanoïque |
Beurre, douce, fromagère, rance |
0,135 |
Acide hexanoïque |
Acre, moisie, fromagère, piquante |
5,4 |
Le seuil de perception de la flaveur « lipolysée » est variable selon les produits laitiers concernés (lait, beurre, crème, fromage) et selon les auteurs. En ce qui concerne le lait, dans le cas d’ajouts dosés d’AGL, il est souvent rapporté l’existence de corrélations entre la teneur en AGL et la perception de la flaveur « rance » ou « lipolysée » par les jurys (Duncan et al., 1991 ; Gonzalez- Cordova et Vallejo-Cordoba, 2003), alors que dans les laits issus de tanks, aucune corrélation n’a été mise en évidence entre ces deux paramètres (Connolly et al., 1979 ; Duncan et al., 1991). Le lait commence à être jugé négativement à partir d’un seuil d’AGL égal à 1,2 mEq/100 g de MG (Connolly et al., 1979 ; Santos et al., 2003). La variabilité des résultats est cependant à prendre en compte. Selon Connolly et al. (1979), 23 % des jurys entraînés sont capables de reconnaître la saveur « lipolysée » à partir de 2,65 mEq/100 g de MG, alors que Santos et al. (2003) rapportaient que 34 % des jurys détectaient cette flaveur au-delà de 1,25 mEq/100 g de MG et 63 % au-delà de 1,75 mEq/100 g de MG. La variabilité des résultats peut s’expliquer par le niveau d’entraînement des jurys, mais également par l’abondance des saveurs retrouvées dans le lait. En effet, il n’y a pas moins de 207 composés volatils (Maarse et Visscher, 1990) qui apportent leur flaveur au lait, avec une synergie variable selon leur concentration. En ce qui concerne les beurres et les crèmes, beaucoup d’études n’ont pas montré de corrélation entre la teneur en AGL et la saveur « lipolysée » (Bell et Parsons, 1977 ; Connolly et al., 1979). Cependant Woo et Lindsay (1983) ont fait le lien entre la teneur en AGL et la flaveur rance. Selon les publications, le seuil de perception de la flaveur « lipolysée » varie entre 0,78 et 2,80 mEq/100 g de MG. Cependant, le seuil de 1,5 mEq/100 g de MG semble être le plus fréquemment utilisé (Woo et Lindsay, 1983 ; Fox et al., 1995). De plus, à ce seuil, les beurres sont susceptibles également d’être plus sensibles à d’autres phénomènes induisant des défauts de flaveur tels que l’oxydation des acides gras. Les AGL sont en effet plus disponibles pour réagir avec d’autres composés (Fox et al., 1995). Selon Nursten (1997) et McNeill et al. (1986), la rancidité des beurres est ressentie à partir de 35 mg/kg de C4:0 et de 26 mg/kg de C6:0, le C4:0 et le C6:0 étant les AGL qui contribuent le plus à la flaveur rance.
b. Fromages
Selon le type de fromages, la contribution des AGL à courtes chaînes, considérés les plus importants, peut être positive ou négative. Dans les fromages dits à lipolyse élevée, tels que les fromages à pâte molle, les fromages italiens à pâte pressée ou les fromages à pâte persillée, le C4:0 apporte une saveur « fromagère », le C6:0 une saveur de « bleu » ou « piquante » et le C8:0 une saveur « fruitée », « chèvre » ou encore « moisie » particulièrement recherchée dans le cas des bleus. Ces AGL sont également les précurseurs de composés volatiles essentiels dans le développement des flaveurs de ces fromages, tels que les méthylcétones, les lactones, les esters et les alcools secondaires. À l’opposé, dans les fromages à lipolyse plus modérée, tels que les fromages à pâte pressée non cuite du type cheddar, gouda, ou cuite du type gruyère ou emmental, les produits de la lipolyse et leurs dérivés participent à la flaveur générale du fromage, mais doivent rester présents en quantité modérée. Dans le cas contraire, le C4:0 est associé à une flaveur « rance » et le C8:0 à une flaveur « savon », « rance » ou « cireuse ». Dans les fromages, les AGL peuvent provenir du lait initial, de l’action de la LPL (si lait cru), des préparations enzymatiques, des ferments et des 30 moisissures apportées au lait lors de la fabrication et l’affinage (tableau 3 ; Fox et al., 1995 ; Wilkinson, 2007).
Pour les fromages dits à lipolyse élevée, 5 à 10 % des TG peuvent être transformés en AGLdans le cas des pâtes molles, et plus de 20 % dans le cas des pâtes persillées. Pour les fromages dits à lipolyse modérée, la lipolyse ne doit pas dépasser 2 % des TG pour éviter le développement de saveurs « rance » ou « lipolysée » (tableau 3 ; Wilkinson, 2007).
Tableau 3. Concentrations en Acides Gras Libres (AGL) totaux présents dans les fromages (adapté de Fox et al., 1995 ; Woo et al., 1984 ; Woo et Lindsey, 1983).
Variété |
AGL (mg/kg) |
Variété |
AGL (mg/kg) |
|---|---|---|---|
Sapsago |
211 |
Gjetost |
1 658 |
Edam |
356 |
Provolone |
2 118 |
Mozzarella |
363 |
Brick |
2 150 |
Colby |
550 |
Limburger |
4 187 |
Camembert |
681 |
Fromage de chèvre |
4 558 |
Port Salut |
700 |
Parmesan |
4 993 |
Monterey Jack |
736 |
Romano |
6 754 |
Cheddar |
1 028 |
Blue mould (US) |
32 230 |
Gruyère |
1 481 |
Roquefort |
32 453 |
1.2. Effet sur la qualité technologique des laits
Certains auteurs ont rapporté des défauts d’aptitude à la transformation des laits à partir d’un certain seuil de lipolyse. Lors de la fabrication du beurre, une lipolyse du lait élevée entraînerait des modifications au niveau du comportement lors de l’écrémage et une augmentation du temps de barattage de la crème (Deeth, 2006 ; Mallia et al., 2008), en lien avec des modifications des capacités moussantes rapportées par Deeth (2006). En effet, les glycérides partiellement hydrolysés présents dans le lait déplaceraient les protéines stabilisatrices de la mousse à l’interface eau/air des bulles formées par le moussage, diminuant les capacités moussantes du lait (Deeth, 2006). Pour le fromage, il a été montré que certains AGL inhiberaient la croissance des bactéries lactiques et des bactéries propioniques utilisées lors de la fabrication et de la maturation des fromages. À titre d’exemple, il a été montré que, même à faible dose (10 à 100 mg/L), les acides gras C12:0, C14:0, C18:0 et C18:3 inhiberaient la croissance du Lactobacillus helveticus et que les acides gras C12:0, C14:0, C18:0 et C18:2 inhiberaient la croissance de Freudenreichii shermani, deux souches très employées en fromagerie (Boyaval et al., 1995).
2. Les mécanismes de la lipolyse du lait de vache
2.1. Le système enzymatique
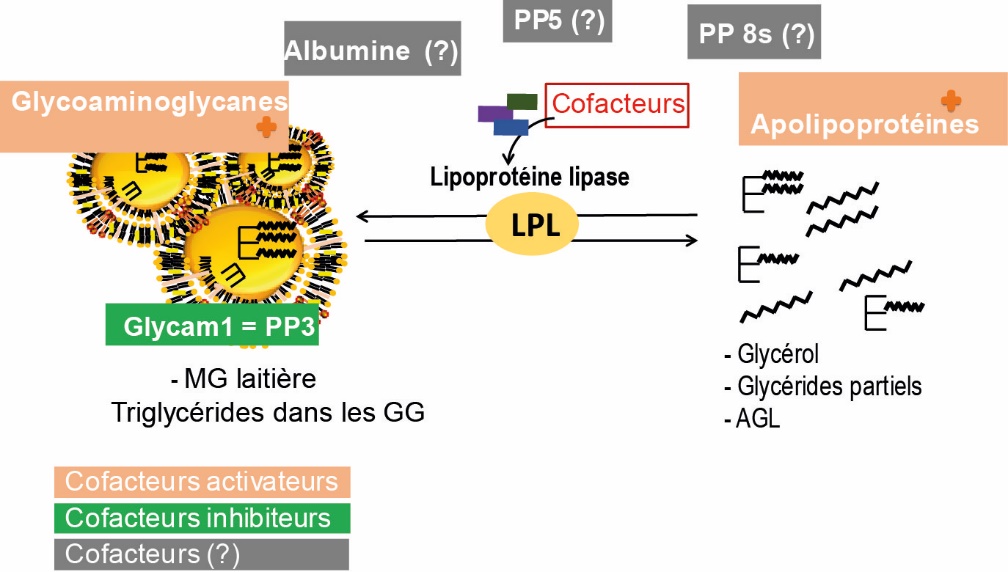
Le système lipolytique (SLi) est le système enzymatique qui conduit à la réaction de lipolyse. Le SLi est constitué par 1) une enzyme native du lait, la LPL, 2) son substrat, les TG constituants les Globules Gras (GG) et 3) ses cofacteurs, activateurs et inhibiteurs. Plusieurs études se sont centrées sur l’identification des différents cofacteurs de la LPL. L’albumine sérique bovine (Deeth et Fitzgerald, 1976 ; Murphy et al., 1979 ; Bengtsson et Olivecrona, 1980), les glycosaminoglycanes du type héparine (Iverius et Ostlund-Lindqvist, 1976) et les apolipoprotéines (Deeth, 2006) ont été identifiés comme de potentiels activateurs de la LPL. La Protéose Peptone (PP) 3 et dans une moindre mesure le composant 8F des PP (Anderson et al., 1981 ; Pâquet, 1989 ; Cartier et al., 1990), la β-lactoglobuline et la lactoferrine (Bläckberg et al., 1979) ont été identifiés comme de potentiels inhibiteurs de la LPL. À noter qu’aucune relation entre l’albumine sérique, le PP8, et la LS n’a été montrée directement dans le lait (Vanbergue et al., 2018b). Le composant 5 des PP a été, quant à lui, identifié dans certaines études comme activateur (Cartier et Chilliard, 1986) et dans d'autres études comme inhibiteur de la LPL (Anderson, 1981 ; Vanbergue et al., 2018b). L’effet activateur de la PP5 est supprimé par la présence de faibles doses de PP3 (Cartier et al., 1990). Finalement, il y a très peu de certitudes concernant les cofacteurs de la LPL. La figure 2 illustre le système enzymatique impliqué dans la réaction de lipolyse du lait.
Figure 2. Système enzymatique impliqué dans la réaction de lipolyse du lait
2.2. Importance du refroidissement du lait
Le refroidissement du lait est un prérequis à l’activation du SLi. En effet, Bengtsson et Olivecrona (1982) ont montré qu’il n’y avait pas de LS dans un lait prélevé manuellement et maintenu à 37°C. La réfrigération permet une réorganisation des composants du lait, propice à la LS, car elle permet de mettre en contact l’enzyme LPL et son substrat, les TG (Cartier et Chilliard, 1990).
a. Évolution de la structure des globules gras
Le refroidissement du lait entraîne une cristallisation fractionnée de la MG, qui se manifeste par une rétractation des GG et une altération de leur membrane (Dickow et al., 2011). Il se produit une exsudation de TG hors du GG, accompagnée d’une agglomération et d’une perte d’intégrité des GG (Dickow et al., 2011), entraînant des modifications de la taille des GG par coalescence. Le refroidissement du lait est également marqué par des phénomènes d’absorption/désorption des composants de la membrane des globules gras (Anderson et al., 1972 ; Badings et Van der Pol, 1973 ; Sundheim et Bengtsson-Olivecrona, 1987b). Plusieurs auteurs ont rapporté un changement de morphologie et d’organisation des domaines lipidiques (Nguyen et al., 2016), accompagné d’une perte des phospholipides de cette membrane. Cette perte est évaluée entre 10 et 18 % selon les auteurs (Patton et al., 1980 ; Evers, 2004), mais reste néanmoins très variable selon les individus (Patton et al., 1980). Le réarrangement des composants de la membrane des GG permet à la LPL d’avoir accès aux TG (Sundheim et Bengtsson-Olivecrona, 1987b). L’évolution de la structure des GG suite à un refroidissement est variable selon la race des vaches laitières (Dickow et al., 2011).
b. La migration de la lipo-protéine lipase à la surface des globules gras
Le refroidissement entraîne également une migration de la LPL, des micelles de caséines vers la surface des GG (Sundheim et Bengtsson-Olivecrona, 1987b ; Dickow et al., 2011). Les déterminants de cette migration sont toutefois peu connus. La réduction de la taille des micelles de caséines et leur plus grande dispersion dans le lait, ainsi que leur solubilisation (essentiellement la caséine β) dans la partie non grasse du lait pourraient, en partie, expliquer ces changements d’interaction entre composants du lait (Dickow et al., 2011). La réorganisation de la membrane des GG précédemment décrite pourrait modifier la liaison entre la LPL et les GG lors de la migration en surface (Dickow et al., 2011).
c. Le rôle des cofateurs de la lipo-protéine lipase
Le comportement des activateurs et inhibiteurs de la LPL, connus ou suspectés (sérum albumine bovine, fraction PP, apolipoprotéines, glycosaminoglycanes) après refroidissement du lait ne sont pas connus.
2.3. Fonctionnement du système enzymatique
En général, l’activité de la LPL est évaluée expérimentalement, dans un milieu en excès de substrat et en présence d’activateurs de l’enzyme (apolipoprotéines du sérum, sérum albumine bovine), à pH alcalin (8,3) et à 37°C ou 39°C. L’activité de la LPL ainsi mesurée représente le potentiel d’activité de la LPL en conditions idéales. L’activité dépend de la quantité de LPL présente et de son efficacité. Elle est donc différente de l’activité de la LPL dans le lait, qui elle dépend de l’équilibre du SLi.
Chez la vache laitière, il n’y aurait pas ou peu de relations entre l’activité de la LPL (mesurée en conditions optimales) et la quantité d’AGL produits dans le lait total (0,15 < R² < 0,4 selon les études ; Bachman et Wilcox, 1990 ; Deeth et Fitzgerald, 1976 ; Ahrné et Björck, 1985 ; Ferlay et al., 2006). La production d’AGL dépend de l’activité de la LPL liée aux GG (R² = 0,65 ; Sundheim, 1988 ; Ahrné et Björck, 1985 ; Cartier et Chilliard, 1990). La corrélation entre la quantité d’AGL et l’activité de la LPL peut également dépendre du moment de la mesure. Une mesure au niveau du plateau enzymatique, lorsque l’enzyme est « saturée » par le substrat, sera indépendante de la quantité et de l’efficacité des enzymes présentes dans le milieu (Cartier et Chilliard, 1990).
Peu de recherches ont porté sur les interactions entre la LPL et le GG (Dickow et al., 2011). Il est néanmoins connu que la LPL se lie aux glycosaminoglycanes du type héparane sulfate, présents à la surface des GG (Dickow et al., 2011). La quantité de ligands (notamment de glycosaminoglycanes) présents à la surface des membranes des GG pourrait expliquer la proportion de LPL présente en surface des GG et finalement la susceptibilité à la lipolyse. Le mode d’action des autres activateurs et inhibiteurs est peu connu. Cependant, il a été observé, lors d’essais in vitro, que la PP 3 n’a pas d’interaction avec la LPL, ni avec les activateurs de la LPL. La PP 3 aurait donc une action inhibitrice, via la protection du substrat grâce à ses propriétés hydrophobes très marquées (Anderson, 1981 ; Cartier et Chilliard, 1986 ; Pâquet, 1989).
En conclusion, d’après Cartier et Chilliard (1990) et Sundheim et Bengtsson-Olivecrona (1987a), les trois facteurs biochimiques déterminants de la sensibilité d’un lait à la LS seraient :
i) l’activité lipasique à la surface des GG ;
ii) l’intégrité et les caractéristiques de la membrane des GG ;
iii) l’équilibre entre facteurs activateurs et facteurs inhibiteurs.
Chacun de ces déterminants peut être modulé par des facteurs intrinsèques à l’animal ou par des facteurs environnementaux (facteurs d’élevage).
3. Les facteurs de variation de la lipolyse spontanée
3.1. Les facteurs de variations de la lipolyse spontanée liés à l’animal
a. L’individu
Chazal et Chilliard (1987a) ont identifié un effet individu important : dans leur essai, 30 à 40 % de la LS étaient expliqués par l’individu et ce résultat était répétable d’une lactation à l’autre. L’effet individu a également été mis en évidence dans la thèse de Vanbergue (2017) avec la description de deux phénotypes de vaches laitières en fonction de leur susceptibilité à présenter des niveaux de LS élevés. Les vaches laitières « non susceptibles » présentaient des niveaux de lipolyse inférieurs à 0,6 mEq/100 g de MG, quelles que soient les conditions environnementales, alors que les vaches laitières « susceptibles » pouvaient présenter des niveaux de lipolyse variables et élevés (> 0,6 mEq/100 g de MG).
b. Le type génétique
Plusieurs études se sont intéressées à l’impact de la race sur le niveau de LS. Chilliard (1982) et Chazal et Chilliard (1987b) n’ont pas observé de différences entre les races Holstein et Montbéliarde. Bachman et al. (1988) ont montré que les vaches Jersiaise étaient moins susceptibles à la LS que les vaches Holstein. Plus récemment, Ferlay et al. (2006) ont montré que les vaches laitières Tarentaise étaient moins susceptibles à la LS que les vaches laitières Montbéliarde. Vanbergue et al. (2017) ont par ailleurs montré que les vaches laitières Normande étaient moins susceptibles à la LS que les vaches laitières Holstein. Cependant, les mécanismes explicatifs de l’effet de la race sont peu décrits et contradictoires dans la littérature. Pour Ferlay et al. (2006), la plus faible susceptibilité de la race Tarentaise à la LS serait liée à la plus grande richesse de son lait en acides gras polyinsaturés. Enfin, des variations de susceptibilité à la LS semblent perceptibles entre différentes populations d’une même race. Jurczak (1995) a constaté une hiérarchisation de la susceptibilité à la LS au sein de la race Holstein, avec une plus forte susceptibilité des Holstein Canadienne et Polonaise comparées aux Holstein Hollandaise, les Holstein Américaine et Néozélandaise ayant des résultats intermédiaires. Chez la vache laitière, la relation entre les variants génétiques et la LS n’a pas encore été étudiée. Cependant, des effets individuels forts et répétables sur plusieurs lactations, ont été mis en évidence (Chazal et Chilliard, 1987a). Chez d’autres ruminants, des effets génétiques ont été mis en évidence. À titre d’exemple chez la chèvre, le polymorphisme du gène CSN1S1, codant pour la caséine αS1, influence les niveaux de LS : des niveaux de LS plus élevés sont observés avec le génotype FF comparé au génotype AA (Chilliard et al., 2014).
c. Le stade physiologique et la parité
Le stade physiologique module les niveaux de LS des vaches laitières susceptibles. La LS serait plus importante en fin de lactation/gestation (Ahrné et Björck, 1985 ; Chazal et Chilliard, 1986 ; Bachman et al., 1988 ; Jurczak, 1995 ; Vanbergue et al., 2017). Chazal et Chilliard (1986) ont notamment observé une augmentation notable de la LS après 32 semaines de lactation, quand le stade de gestation est supérieur à 24 semaines et que la production laitière est faible. L’importance relative de ces trois paramètres est difficile à déterminer, car ils sont souvent en interaction. D’après Chazal et Chilliard (1986), le stade de gestation est le principal responsable de l’augmentation de la LS en fin de lactation. L’augmentation de la libération d’hormones (œstrogènes, progestérone) après le 4ème mois et après le 6ème mois de gestation pourrait être responsable de cette variation de la LS (Jurczak, 1995). Cela a été observé lors d’injection d’œstrogènes aux vaches laitières (Bachman, 1982 ; Cartier et Chilliard, 1994). Le niveau de production laitière semble également influencer le niveau de LS au-delà de l’effet du stade physiologique, car avant même la 24ème semaine de gestation, Chazal et Chilliard (1987c), ont constaté une forte augmentation de la LS en lien avec la diminution de production laitière. Plus récemment, une augmentation de la LS chez des vaches laitières hautes productrices en début de lactation a été montrée par Vanbergue et al. (2017). Selon ces auteurs, le bilan énergétique négatif en lien avec la priorisation de la fonction de lactation par ces vaches laitières lors de l’allocation de l’énergie pourrait expliquer l’augmentation des niveaux de LS. Ces effets sont plus marqués chez les multipares, probablement en lien avec une production laitière plus importante. En milieu et en fin de lactation, Vanbergue et al. (2017) ont rapporté des niveaux de LS inférieurs chez les vaches laitières multipares comparés aux primipares, en accord avec Connolly (1978) et Chilliard et Lamberet (1984).
3.2. Les facteurs de variations de la lipolyse spontanée liés à la conduite de l’animal et à son environnement
a. Le moment de la traite et les intervalles entre traites
Le moment de la traite a été identifié dans plusieurs publications comme facteur de variation des niveaux de LS. Murphy et al. (1979), Jellema (1975), Ahrné et Björck (1985) et plus récemment Vanbergue et al. (2017), ont montré que la LS était plus importante dans le lait de la traite du soir que dans celui de la traite du matin. La différence observée entre le matin et le soir pourrait être due aux durées d’intervalles de traite et aux différences de quantité de lait produite entre le matin et le soir. En effet, avec des intervalles égaux entre les deux traites, Bachman et al. (1988) n’ont pas observé de différence de niveaux de LS entre les laits des traites du matin et du soir.
b. La fréquence de traite
L’augmentation de la fréquence de traite est accompagnée d’une augmentation de la LS du lait. Comparé à un système de traite biquotidienne, classiquement rencontré en élevage bovin français, la monotraite entraîne une diminution drastique de la LS (268 %) (Pomiès et al., 2007 ; Vanbergue et al., 2016) alors que la traite trois à quatre fois par jour entraîne une augmentation de la LS, quel que soit le stade de lactation (+ 20 à + 23,5 % ; Wiking et al., 2006). Les mécanismes responsables de ces variations seraient plutôt des mécanismes locaux, impliquant la glande mammaire, que des mécanismes systémiques, puisque ces variations sont observables lors d’application de fréquences de traite différentes entre les demi-mamelles (Wiking et al., 2006). Il pourrait également y avoir un effet des quantités de lait produites plus faibles à chaque traite lors de traites multiples sur une même journée. Des variations d’activité lipasique et du nombre de transcrits pour le gène LPL, en lien avec des variations de fréquence de traite (Pomiès et al., 2007 ; Boutinaud et al., 2013), pourraient expliquer ces effets de la fréquence de traite.
c. L’alimentation
La nature du fourrage influence les variations de LS. En effet, lorsque les vaches laitières sont au pâturage, la LS est plus faible (Deeth et Fitzgerald, 1976 ; Chazal et al., 1987 ; Vanbergue et al., 2017). Un foin de bonne qualité, utilisé comme fourrage principal est également généralement associé à des niveaux de LS bas (Deeth et Fitzgerald, 1976 ; Chazal et al., 1987). L’utilisation d’ensilage d’herbe comme fourrage principal augmenterait les niveaux de LS, comparativement à l’herbe fraîche (+ 130 %) et au foin (+ 93 %) (Chazal et al., 1987 ; Ferlay et al., 2006). Les effets de l'ensilage de maïs sont variables dans la littérature. Dans une étude de Ferlay et al. (2006), l’ensilage de maïs est associé à des niveaux de LS plus faibles que l’herbe conservée, alors que dans une étude de Vanbergue et al. (2018b), l’ensilage de maïs est associé à des niveaux de LS plus élevés. Ces différences pourraient être expliquées par les différentes races de vaches laitières impliquées dans ces deux études ou par le déficit en PDI de la ration chez Vanbergue et al. (2018b). Cette hypothèse est corroborée par les résultats de Hurtaud et al. (2018) qui ont montré que des rations avec des niveaux bas de matières azotées totales (9 vs 18 %) entraînaient une augmentation de la LS.
L’effet d’une restriction alimentaire (– 10 à – 25 % des apports) sur les niveaux de LS a également été étudié dans la littérature. Vanbergue et al. (2017) ont montré qu’une restriction alimentaire (– 20 à – 25 % des quantités ingérées à volonté) entraînait une augmentation de la LS, quel que soit le stade de lactation. Un bilan énergétique négatif, entrainerait une augmentation des niveaux de LS. Une réduction de 38 % de l’accessibilité au pâturage n’a pas d’incidence sur la LS (Thomson et al., 2005), alors qu’une restriction alimentaire (-10 à – 20 % des apports) dans le cadre d’une alimentation à base de fourrages conservés entraîne une dégradation de la LS des vaches laitières (Jellema, 1975 ; Chilliard, 1982). L’effet de la restriction alimentaire aurait tendance à être plus marqué lorsque que les vaches laitières sont alimentées à base d'herbe conservée par rapport à l’ensilage de maïs (Vanbergue et al., 2018b). Les effets de la restriction alimentaire seraient plus marqués en fin de lactation (Deeth et Fitzgerald, 1976 ; Connolly, 1978 ; O'Brien et al., 1996).
Hurtaud et al. (2010), et Vanbergue et al. (2018a) ont montré qu’une supplémentation en huile de colza, en lin extrudé (3,1 % de la matière sèche ingérée) et en micro-algues (2,5 % de la matière sèche ingérée) entraînait une augmentation de la LS, alors que Vanbergue et al. (2018a) ont montré qu’une supplémentation en lin extrudé (2,5 % de la matière sèche ingérée) entraînait une diminution de la LS. Les suppléments lipidiques ont un effet variable sur la LS, qui semble dépendre de leur impact sur le fonctionnement ruminal. La forme et la dose du supplément lipidique semblent être déterminantes sur les variations du fonctionnement ruminal (Vanbergue et al., 2017).
d. La saison
Même si des variations saisonnières sont observées dans les élevages Français, avec un pic de LS observé l’été (Vanbergue et al., 2017), aucune étude n’a porté sur l’évaluation de l’effet de la saison (température, photopériode).
4. La lipolyse induite
La Lipolyse Induite (LI) est due à des altérations mécaniques ou thermiques du lait, pendant la traite, le stockage et la transformation. Chaque facteur pris séparément n’a pas forcément un impact important, mais le cumul de ces différents facteurs entraîne souvent une augmentation notable de la lipolyse.
Les travaux de Cartier et Chilliard (1989) attestent que les laits les plus sensibles, avec des niveaux de LS déjà élevés, seraient les plus impactés par la LI. Cette relation est dépendante de la saison (Chazal et Chilliard, 1987b), probablement en raison d’une interaction avec la température ambiante lors de l’induction mécanique de la lipolyse.
4.1. Effets mécaniques
Les altérations mécaniques en ferme peuvent être consécutives à des brassages, aérations ou moussages du lait. Lors des brassages, les membranes des GG sont fragilisées, voire éclatent, facilitant l’action des lipases présentes dans le lait. Ces brassages favorisent également la migration des lipases, des micelles de caséine, via le sérum, vers les globules gras (Cartier, 1987). Lors des aérations et moussage du lait, les GG sont étalés sur les bulles d’air, ce qui engendre une déformation et une fragilisation de leurs membranes, facilitant l’action des lipases.
Tout ce qui peut conduire à un écoulement autre que stable et laminaire dans le lactoduc de traite pourra avoir un effet sur les résultats : coudes trop serrés, contrepentes ou remontées, réduction du diamètre ou longueur excessive. Chaque élément présent sur le circuit du lait aura tendance à augmenter le niveau de lipolyse induite, avec un effet cumulatif.
Diverses études (Fleming, 1980) conduisent systématiquement à des résultats de lipolyse se dégradant progressivement, en passant de la traite manuelle, à la traite au pot (0,55 mEq/100 g de MG), en lactoduc en ligne basse (0,65 mEq/100 g de MG) et avec enfin des résultats les plus élevés en ligne haute (0,85 mEq/100 g de MG).
Il y a peu de différences entre chacun des éléments constitutifs d’une installation de traite, ou entre mêmes éléments de marques différentes, fonctionnant correctement. L’effet moyen des faisceaux trayeurs est par exemple de + 0,11 à 0,18 mEq/100 g de MG (Heuchel, 1994). Par contre, en cas de consommations exagérées d’air des faisceaux trayeurs, les résultats peuvent facilement doubler. De même, le positionnement ou la configuration de cette entrée d’air, nécessaires pour une co-circulation efficace air-lait, peuvent modifier l’impact lipolyse d’un faisceau trayeur.
Le barattage du lait peut également se produire en cas de désamorçage de la pompe à lait, si la chambre de réception est complétement vidangée (Heuchel, 1994). Cela favorise la cavitation, et donc l’incorporation d’air au lait (+ 30 % de LI). Chaque chambre de réception a donc un volume utile, différence entre un volume maximal et minimal de déclenchement de son fonctionnement.
Avec les robots de traite, on a toujours constaté des résultats (LS + LI) en moyenne plus élevés qu’en traite conventionnelle (+ 39 %), ceci étant lié à des consommations d’air proportionnellement plus importantes et à un circuit de lait plus complexe. Les matériels évoluent (moins de consommations d’air, circuit de lait optimisé), notamment pour corriger ce défaut de qualité du lait. Néanmoins, une étude menée sur 43 élevages robotisés bretons par Fleuret et al. (2014) montrait toujours une dégradation des résultats lipolyse pour 64 % d’entre eux après arrivée du robot, avec une augmentation moyenne, de + 0,25 mEq/100 g de MG et 44 % des élevages étaient pénalisés (contre 11 % auparavant).
L’agitation du lait dans le tank peut également théoriquement influencer la LI, notamment lors de la première traite après vidange. Elle peut générer de la turbulence et du moussage du lait, facilitant l’action des lipases. Malgré tout, les impacts semblent limités et non significatifs (Heuchel, 1996).
4.2. Inductions thermiques
La lipolyse augmente en cas de refroidissement lent (Willart et Sjöström, 1966 ; Fleming, 1980). Elle augmente également avec l’allongement de la durée de stockage (Cartier, 1987). L’impact de succession de séquences de refroidissement-réchauffement est plus important (Cartier, 1987 ; Fleming, 1980). Ces effets sont surtout valables pour des laits déjà sensibles.
La première traite après vidange du tank est en général plus pénalisée que les autres (Heuchel, 1996), avec plus de variations de température, un effet assez limité de la possible congélation du lait, qu’il convient néanmoins d’éviter. Les traites suivantes auront un effet s’il y a des fortes fluctuations de température (Heuchel, 1996), a minima de 15°C et maximale au-delà de 25°C. La mise en place d’un pré-refroidisseur permet en général de limiter les risques, notamment sur des exploitations à facteurs de risque élevés (Heuchel, 1990).
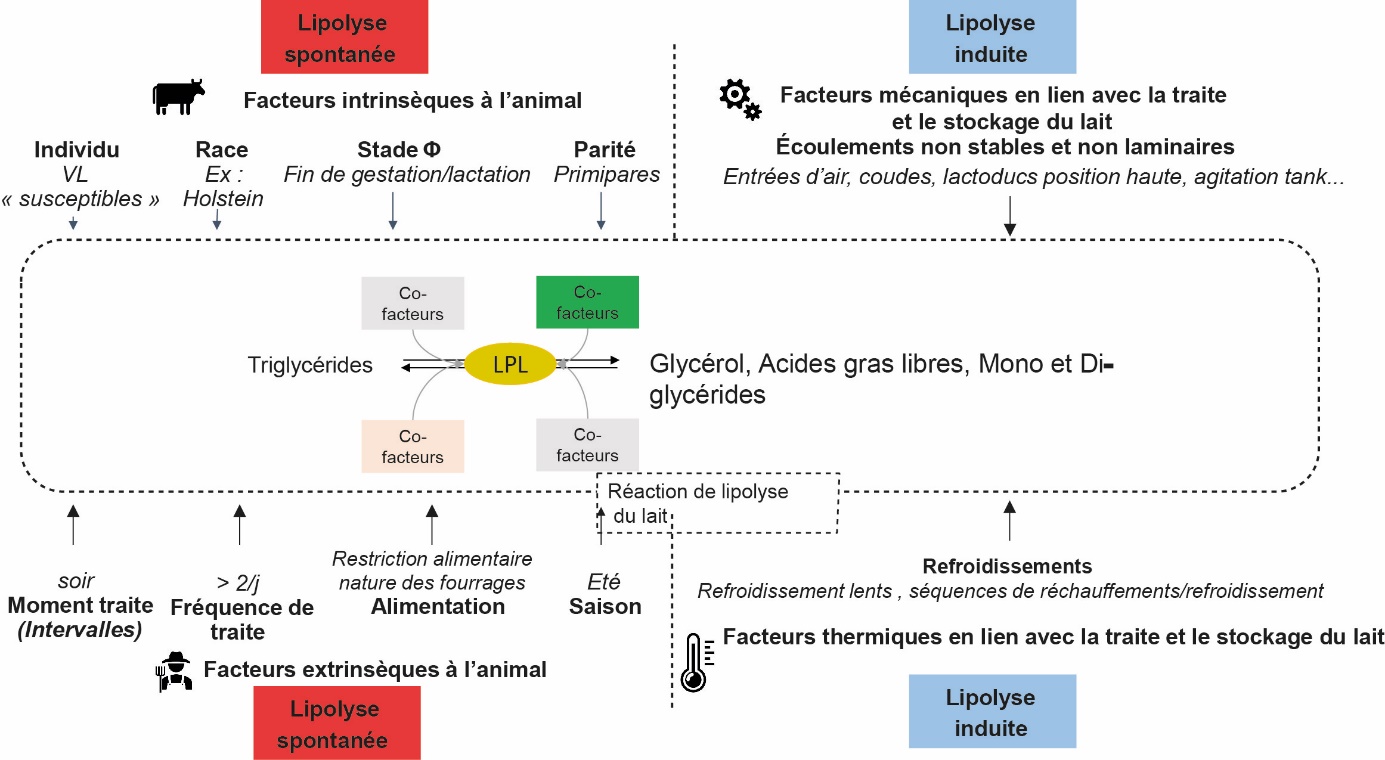
Figure 3. Facteurs induisant une augmentation de la lipolyse spontanée et induite.
Conclusion
En France, la lipolyse est étudiée avec attention car elle influence les qualités organoleptiques et technologiques du lait et des produits laitiers. Dans certaines régions, la lipolyse fait partie des critères de paiement du lait. La limite à ne pas dépasser est fixée à 0,89 mEq/100 g MG. Hors problèmes sanitaires, dans les premières 48 h qui suivent la traite, la lipolyse mesurée dans le tank est le reflet de la combinaison entre la lipolyse spontanée et induite. La figure 3 résume les facteurs induisant une augmentation de la lipolyse spontanée et induite.
La susceptibilité des vaches laitières du troupeau à la lipolyse conditionne les fluctuations de la lipolyse dans le tank. Les vaches dites « non susceptibles » présentent un taux de lipolyse individuel faible et stable pendant leur carrière alors que les vaches dites « susceptibles » présentent un taux de lipolyse fluctuant de faible à très élevé, en fonction des facteurs d’élevage, de l’installation de traite et du stockage du lait. La LS dépend de facteurs intrinsèques à l’animal, tels que la race, le stade physiologique (lactation/gestation), la parité, et de facteurs de conduite et d’environnement, tels que l’alimentation, la fréquence de traite, l’intervalle entre traite et la saison. Les vaches de race Holstein semblent plus susceptibles à la lipolyse, comparées à la Normande ou à la Tarentaise. Même si la hiérarchisation des facteurs de risques reste complexe, les modalités en lien avec une forte augmentation de la lipolyse parmi les vaches susceptibles sont : le stade de gestation (à partir de 6/7 mois), l’augmentation de la fréquence de traite (x3/j), la traite du soir (dans le cas d’un intervalle de traite 10 h/14 h), le niveau de production laitière par traite. Une attention particulière doit être apportée à la satisfaction des besoins alimentaires (énergie, azote) surtout chez les fortes productrices en début de lactation. Le pâturage semble être associé à des niveaux de lipolyse plus faibles.
Dans le cadre d’un fonctionnement normal des installations de traite, quelle que soit la marque, il y a peu d’effet de chacun des éléments constitutifs d’une installation de traite (faisceaux trayeurs, lactoduc, pompe à lait, chambre de réception, tank), mais le cumul des effets faibles de ces différents facteurs peut entraîner une augmentation notable de la lipolyse. La présence de dysfonctionnements dans le circuit du lait multiplie l’impact des éléments concernés. Sur les robots de traite, la lipolyse est en moyenne plus élevée qu’en traite conventionnelle. Cependant, les matériels évoluent pour corriger ce défaut de qualité du lait (moins de consommation d’air, circuits de lait optimisés).
Selon les systèmes d’élevage, plusieurs leviers sont donc disponibles pour minimiser la lipolyse : sélection de vaches « non susceptibles », ration équilibrée, tarissement à 6/7 mois de gestation, entretien des installations de traite.
D’un point de vue mécanistique, plusieurs hypothèses ont été avancées pour expliquer la sensibilité d’un lait à la lipolyse. Les trois facteurs biochimiques déterminants de la sensibilité d’un lait à la lipolyse seraient : l’activité lipasique à la surface des GG, l’intégrité et les caractéristiques de la membrane des GG (fragilité des membranes), l’équilibre entre facteurs activateurs et facteurs inhibiteurs. Leurs influences respectives demandent encore à être précisées.
Références
- Ahrné L., Björck L., 1985. Lipolysis and the distribution of lipase activity in bovine milk in relation to stage of lactation and time of milking. J. Dairy Res., 52, 55-64.
- Anderson M., 1981. Inhibition of lipolysis in bovine milk by proteose peptone. J. Dairy Res., 48, 247-252.
- Bachman K.C., 1982. Effect of exogenous estradiol and progesterone upon lipase activity and spontaneous lipolysis in bovine milk. J. Dairy Sci., 65, 907-914.
- Bachman K.C., Wilcox C.J., 1990. Effect of blood and high density lipoprotein preparations upon lipase distribution and spontaneous lipolysis in bovine milk. J. Dairy Sci., 73, 3393- 3401.
- Bachman K.C., Hayen M.J., Morse D., Wilcox C.J., 1988. Effect of pregnancy, milk yield, and somatic cell count on bovine milk fat hydrolysis. J. Dairy Sci., 71, 925-931.
- Badings H.T., Van der Pol J.J.G., 1973. Effect of cooling milk on the heat-release of hydrogen sulphide from the fat-globule membrane. Nederlands melk-en zuiveltijdschrift, 27, 45-53.
- Bell L.I., Parsons J.G., 1977. Factors affecting lipase flavor in butter. J. Dairy Sci., 60, 117-122.
- Bendall J.G., 2001. Aroma compounds of fresh milk from New Zealand cows fed different diets. J. Agri. Food Chem., 49, 4825-4832.
- Bengtsson G., Olivecrona T., 1980. Lipoprotein lipase: Some effects of activator proteins. Eur. J. Biochem., 106, 549-555.
- Bengtsson G., Olivecrona T., 1982. Activation of lipoprotein lipase by apolipoprotein CII. FEBS letters, 147, 183-187.
- Bläckberg L., Hernell O., Bengtsson G., Olivecrona T., 1979. Colipase enhances hydrolysis of dietary triglycerides in the absence of bile salts. J. Clin. Invest., 64, 1303-1308.
- Boutinaud M., Galio L., Lollivier V., Finot L., Wiart S., Esquerre D., Devinoy E., 2013. Unilateral once daily milking locally induces differential gene expression in both mammary tissue and milk epithelial cells revealing mammary remodeling. Physiol. Genomics, 45, 973-985.
- Boyaval P., Corre C., Dupuis C., Roussel E., 1995. Effect of free fatty acids on propionic acid bacteria. Lait, 75, 17-29.
- Cartier P., 1987. Aspects biochimiques de la lipolyse spontanée du lait de vache. Thèse. Université de Clermont II.
- Cartier P., Chilliard Y., 1986. Effects of different skim milk fractions on activity of cow milk purified lipoprotein lipase. J. Dairy Sci., 69, 951-955.
- Cartier P., Chilliard Y., 1989. Lipase redistribution in cows' milk during induced lipolysis. I. Activation by agitation, temperature change, blood serum and heparin. J. Dairy Res., 56, 699-709.
- Cartier P., Chilliard Y., 1990. Spontaneous lipolysis in bovine milk: combined effects of nine characteristics in native milk. J. Dairy Sci., 73, 1178-1186.
- Cartier P., Chilliard Y., 1994. Effects of estradiol injection on milk composition, milk fat lipolysis and lipase activity in the non-pregnant dairy cows. Ann. Zoot. 43(suppl. 1), 45S.
- Cartier P., Chilliard Y., Pâquet D., 1990. Inhibiting and activating effects of skim milks and proteose-peptone fractions on spontaneous lipolysis and purified lipoprotein lipase activity in bovine milk. J. Dairy Sci., 73, 1173-1178.
- Chazal M.-P., Chilliard Y., 1986. Effect of stage of lactation, stage of pregnancy, milk yield and herd management on seasonal variation in spontaneous lipolysis in bovine milk. J. Dairy Res., 53, 529-538.
- Chazal M.P., Chilliard Y., 1987a. Les variations individuelles de la lipolyse spontanée du lait de vache : effet du numéro de lactation et répétabilité au cours de deux lactations successives. Lait, 67, 437-450.
- Chazal M.P., Chilliard Y., 1987b. Effect of breed of cow (Friesian and Montbeliarde) on spontaneous and induced lipolysis in milk. J. Dairy Res., 54, 7-11.
- Chazal M.P., Chilliard Y., 1987c. Effets respectifs du stade de lactation, du stade de gestation et du niveau de production sur la lipolyse spontanée du lait de vache. Lait, 67, 379-392.
- Chazal M.P., Chilliard Y., Coulon J.B., 1987. Effect of nature of forage on spontaneous lipolysis in milk from cows in late lactation. J. Dairy Res., 54, 13-18.
- Cheng H.F., 2010. Volatile flavor compounds in yogurt: A review. Crit. Rev. Food Sci. Nutr., 50, 938-950.
- Chilliard Y., 1982. Variations physiologiques des activités lipasiques et de la lipolyse spontanée dans les laits de vache, de chèvre et de femme: revue bibliographique. Lait, 62, 1-31.
- Chilliard Y., Lamberet G., 1984. Milk lipolysis - various types, mecanisms, factors of variation, practical significance. Lait, 64, 544-578.
- Chilliard Y., Toral P.G., Shingfield K.J., Rouel J., Leroux C., Bernard L., 2014. Effects of diet and physiological factors on milk fat synthesis, milk fat composition and lipolysis in the goat: A short review. Small Rum. Res., 122, 31-37.
- Chouinard Y., Villeneuve M., Lebeuf Y., Tremblay F., Gervais R., 2012. Facteurs alimentaires modulant le profil aromatique du lait chez la vache, 36ème symposium sur les bovins laitiers.
- Connolly J.F., 1978. Recent findings on lipolysis in Ireland. The impact of environment and nutrition on free fatty acids and flavour in milk and dairy products. In: 20. Int. Dairy Congr., Paris, France.
- Connolly J.F., Murphy J.J., O'Connor C.B., Headon D.R., 1979. Relationship between lipolysed flavour and free fatty acid levels in milk and butter. Irish J. Food Sci. Technol., 3, 79-92.
- Deeth H.C., 2006. Lipoprotein lipase and lipolysis in milk. Int. Dairy J., 16, 555-562.
- Deeth H.C., Fitzgerald C.H., 1976. Lipolysis in dairy products: A review. Australian J. Dairy Technol., 31, 53-64.
- Dickow J.A., Larsen L.B., Hammershøj M., Wiking L., 2011. Cooling causes changes in the distribution of lipoprotein lipase and milk fat globule membrane proteins between the skim milk and cream phase. J. Dairy Sci., 94, 646-656.
- Duncan S.E., Christen G.L., Penfield M.P., 1991. Rancid flavor of milk, relationship of acid degree value, free fatty acids and sensory perception. J. Food Sci., 56, 394-397.
- Evers J.M., 2004. The milkfat globule membrane—compositional and structural changes post secretion by the mammary secretory cell. Int. Dairy J., 14, 661-674.
- Ferlay A., Martin B., Pradel P., Coulon J.B., Chilliard Y., 2006. Influence of grass-based diets on milk fatty acid composition and milk lipolytic system in tarentaise and Montbeliarde cow breeds. J. Dairy Sci., 89, 4026-4041.
- Fleming M.G., 1980. Facteurs mécaniques associés à la lipolyse dans le lait de vache. In : Anomalies du gout du lait et des produits laitiers dues à la lipolyse. Bull. FIL, 118, 44-55.
- Fleuret M., Merlhe M., François J., Guiocheau S., 2014. Résultats techniques et économiques de deux échantillons d’élevages français avec ou sans robot de traite. Incidence de la part de pâturage chez ceux équipés d’un robot. Renc. Rech. Rum., 21, 355
- Fox P.F., Singh T.K., McSweeney P.L.H., 1995. Biogenesis of flavour compounds in cheese. In: Chemistry of Structure-Function Relationships in Cheese. Malin E.L., Tunick M.H. (Eds). Springer US, Boston, MA, 59-98.
- Gonzalez-Cordova A.F., Vallejo-Cordoba B., 2003. Detection and prediction of hydrolytic rancidity in milk by multiple regression analysis of short-chain free fatty acids determined by solid phase microextraction gas chromatography and quantitative flavor intensity assessment. J. Agri. Food Chem., 51, 7127-7131.
- Heuchel V., 1990. Faut-il prérefroidir le lait ? Annuel pour l'éleveur bovin. Institut de l'Élevage, Paris, France. 12, 57-64.
- Heuchel V., 1994. Mesure de l'incidence de différents types de faisceaux trayeurs sur la lipolyse du lait de vache. In : Facteurs d’élevage influençant la qualité du lait, Idele - Inra (Eds). 1ère Renc. Rech. Rum., Paris, France, 125-128.
- Heuchel V., 1996. Incidence sur la lipolyse des conditions d'agitation du lait pendant son stockage à la ferme. Compte rendu d'essais n° 96071. Institut de l'Elevage, Paris, France. 8 p.
- Heuchel V., Chilliard Y., 1988. Le point sur la lipolyse du lait de vache. Institut Technique de l’Élevage Bovin, France. 35p.
- Hurtaud C., Faucon F., Couvreur S., Peyraud J.L., 2010. Linear relationship between increasing amounts of extruded linseed in dairy cow diet and milk fatty acid composition and butter properties. J. Dairy Sci., 93, 1429-1443.
- Hurtaud C., Riosa R., Brégeron S., Suzanne A., Edouard N., 2018. Effect of milking time, temperature and diet nitrogen level on milk composition of dairy cows and on some milk properties (freezing point, lipolysis and heat stability). In: 10. International Symposium on the Nutrition of Herbivores (ISNH). Cambridge University Press, Clermont-Ferrand, France,
- Iverius P.H., Ostlund-Lindqvist A.M., 1976. Lipoprotein lipase from bovine milk. Isolation procedure, chemical characterization, and molecular weight analysis. J. Biol. Chem., 251, 7791-7795.
- Jellema A., 1975. Note on susceptibility of bovine milk to lipolysis. Neth. Milk Dairy J., 29, 145-152.
- Jurczak M.E., 1995. The effect of genetic factors, stage of lactation, season and feeding system on fat lipolysis in raw milk of Black-and-White cows and F 1 crosses of that breed with bulls of 4 varieties of Friesian cattle. Ann. Warsaw Agricult. Univ., Anim. Sci., 17.
- Maarse H., Visscher C.A., 1990. Volatile compounds in food: qualitative and quantitative data: supplement and cumulative index. TNO-CIVO Food Analysis Institute, Zeist, Netherlands.
- Mallia S., Escher F., Schlichtherle-Cerny H., 2008. Aroma-active compounds of butter: A review. Eur. Food Res. Technol., 226, 315-325.
- McDaniel M.R., Sather L.A., Lindsay R.C., 1969. Influence of free fatty acids on sweet cream butter flavor. J. Food Sci., 34, 251-254.
- McNeill G.P., O'Donoghue A., Connolly J.F., 1986. Quantification and identification of flavour components leading to lipolytic rancidity in stored butter. Irish J. Food Sci. Technol., 10, 1-10.
- Moio L., Dekimpe J., Etievant P., Addeo F., 1993. Neutral volatile compounds in the raw milks from different species. J. Dairy Res., 60, 199-213.
- Murphy J.J., Connolly J.F., Headon D.R., 1979. A study of factors associated with free fatty acid development in milk. Irish J. Food Sci. Technol., 3, 131-149.
- Nguyen H.T.H., Madec M.N., Ong L., Kentish S.E., Gras S.L., Lopez C., 2016. The dynamics of the biological membrane surrounding the buffalo milk fat globule investigated as a function of temperature. Food Chem., 204, 343-351.
- Nursten H.E., 1997. The flavour of milk and dairy products .1. Milk of different kinds, milk powder, butter and cream. Int. J. Dairy Technol., 50, 48-56.
- O'Brien B., Crosse S., Dillon P., 1996. Effects of offering a concentrate or silage supplement to grazing dairy cows in late lactation on animal performance and on milk processability. Irish J. Agri. Food Res., 35, 113-125.
- Pâquet D., 1989. Review: the proteose-peptone fraction of milk. Lait, 69, 1-21.
- Patton S., Long C., Sooka T., 1980. Effect of storing milk on cholesterol and phospholipid of skim milk. J. Dairy Sci., 63, 697-700.
- Pomiès D., Martin B., Chilliard Y., Pradel P., Rémond B., 2007. Once-a-day milking of Holstein and Montbéliarde cows for 7 weeks in mid-lactation. Animal, 1, 1497-1505.
- Santos M.V., Ma Y., Caplan Z., Barbano D.M., 2003. Sensory threshold of off-flavors caused by proteolysis and lipolysis in milk. J. Dairy Sci., 86, 1601-1607.
- Scanlan R.A., Sather L.A., Day E.A., 1965. Contribution of free fatty acids to flavor of rancid milk. J. Dairy Sci., 48, 1582-1586.
- Shipe W.F., Bassette R., Deane D.D., Dunkley W.L., Hammond E.G., Harper W.J., Kleyn D.H., Morgan M.E., Nelson J.H., Scanlan R.A., 1978. Off flavors of milk: nomenclature, standards, and bibliography. J. Dairy Sci., 61, 855-869.
- Shipe W.F., Senyk G.F., Fountain K.B., 1980. Modified copper soap solvent extraction method for measuring free fatty acids in milk. J. Dairy Sci., 63, 193-198.
- Sundheim G., 1988. Spontaneous lipolysis in bovine milk with special reference to lipoprotein lipase and its mode of action in milk. 8p.
- Sundheim G., Bengtsson-Olivecrona G., 1987a. Hydrolysis of Bovine Milk Fat Globules by Lipoprotein Lipase: Inhibition by Proteins Extracted from Milk Fat Globule Membrane. J. Dairy Sci., 70, 1815-1821.
- Sundheim G., Bengtsson-Olivecrona G., 1987b. Methods to assess the propensity of milk fat globules toward lipolysis and the ability of skim milk to inhibit lipolysis. J. Dairy Sci., 70, 2040-2045.
- Thomson N.A., Van der Poel W.C., Woolford M.W., Auldist M.J., 2005. Effect of cow diet on free fatty acid concentrations in milk. NZ J. Agri. Res., 48, 301-310.
- Vanbergue E., 2017. Les facteurs de variations de la lipolyse spontanée du lait de vache et mécanismes biochimiques associés. Thèse. Agrocampus Ouest.
- Vanbergue E., Peyraud J.L., Guinard-Flament J., Charton C., Barbey S., Lefebvre R., Gallard Y., Hurtaud C., 2016. Effects of DGAT1 K232A polymorphism and milking frequency on milk composition and spontaneous lipolysis in dairy cows. J. Dairy Sci., 99, 5739-5749.
- Vanbergue E., Delaby L., Peyraud J.L., Colette S., Gallard Y., Hurtaud C., 2017. Effects of breed, feeding system, and lactation stage on milk fat characteristics and spontaneous lipolysis in dairy cows. J. Dairy Sci., 100, 4623-4636.
- Vanbergue E., Peyraud J.L., Hurtaud C., 2018a. Effects of new n-3 fatty acid sources on milk fatty acid profile and milk fat properties in dairy cows. J. Dairy Res., 85, 265-272.
- Vanbergue E., Peyraud J.L., Ferlay A., Miranda G., Martin P., Hurtaud C., 2018b. Effects of feeding level, type of forage and milking time on milk lipolytic system in dairy cows. Liv. Sci., 217, 116-126.
- Wiking L., Nielsen J.H., Båvius A.K., Edvardsson A., Svennersten-Sjaunja K., 2006. Impact of milking frequencies on the level of free fatty acids in milk, fat globule size, and fatty acid composition. J. Dairy Sci., 89, 1004-1009.
- Wilkinson M.G., 2007. Lipolysis and cheese flavour development. In: Improving the Flavour of Cheese. Weimer B.C. (Ed). Woodhead Publ Ltd, Cambridge, 102-120.
- Willart S., Sjöström G., 1966. The effect of cooling and freezing on the lipolysis in raw milk. 17th Int. Dairy Congr., A, 287.
- Woo A.H., Kollodge S., Lindsay R., 1984. Quantification of major fatty acides in several cheese varieties. J. Dairy Sci., 67,874-878.
- Woo A.H., Lindsay R.C., 1983. Statistical correlation of quantitative flavor intensity assessments and individual free fatty acid measurements for routine detection and prediction of hydrolytic rancidity off-flavors in butter. J. Food Sci., 48, 1761-1766.
Résumé
La lipolyse est une réaction enzymatique qui influence négativement les qualités organoleptiques et technologiques du lait. Dans certaines régions de France, la lipolyse est un critère de paiement du lait. La susceptibilité des vaches à la lipolyse conditionne les fluctuations de la lipolyse dans le tank. Les vaches dites « non susceptibles » présentent un taux de lipolyse individuel faible et stable pendant leur carrière alors que les vaches dites « susceptibles » présentent un taux de lipolyse fluctuant de faible à très élevé, en fonction des facteurs d’élevage, de l’installation de traite et du stockage. Selon les systèmes d’élevage, plusieurs leviers sont disponibles pour minimiser la lipolyse : sélection de vaches « non susceptibles » à la lipolyse parmi les vaches Holstein ou recours à d’autres races de vaches moins « susceptibles » telles que les vaches de race Normande ou Tarentaise à titre d’exemple, tarissement à 6 mois de gestation pour les vaches « susceptibles », maintien de la fréquence de traite à deux traites par jour. Une attention particulière doit être accordée à l’équilibre des rations (énergie, azote) et à la complémentation (lipides) surtout chez les vaches fortes productrices en début de lactation. Le pâturage semble être associé à des niveaux de lipolyse faibles. Un bon entretien des installations de traite doit être réalisé car la présence de dysfonctionnements multiplie l’impact du circuit de traite sur la lipolyse. Avec les robots de traite, la lipolyse est en moyenne plus élevée qu’en traite conventionnelle, cependant l’amélioration des matériels est continue. Les mécanismes biochimiques, explicatifs de la lipolyse sont toujours à l’étude.)
Pièces jointes
Pas de document complémentaire pour cet articleStatistiques de l'article
 Vues: 24674
Vues: 24674
Téléchargements
 PDF: 1463
PDF: 1463
 XML: 175
XML: 175
Articles les plus lus par le même auteur ou la même autrice
- Sarah LAISSE, René BAUMONT, Léonie DUSART, Didier GAUDRÉ, Benoit ROUILLÉ, Marc BENOIT, Patrick VEYSSET, Didier RÉMOND, Jean-Louis PEYRAUD, L’efficience nette de conversion des aliments par les animaux d’élevage : une nouvelle approche pour évaluer la contribution de l’élevage à l’alimentation humaine , INRAE Productions Animales: Vol. 31 No 3 (2018): Volume 31 Numéro 3 : Dossier : Ressources alimentaires pour les animaux d'élevage
- Jean-Louis PEYRAUD, Joël AUBIN, Marc BARBIER, René BAUMONT, Cécile BERRI, Jean-Pierre BIDANEL, Christine CITTI, Corinne COTINOT, Christian DUCROT, Pierre DUPRAZ, Philippe FAVERDIN, Nicolas FRIGGENS, Sabine HOUOT, Marie-Odile NOZIÈRES-PETIT, Claire ROGEL-GAILLARD, Véronique SANTÉ-LHOUTELLIER, Quelle science pour les élevages de demain ? Une réflexion prospective conduite à l’INRA , INRAE Productions Animales: Vol. 32 No 2 (2019): Volume 32 Numéro 2 : Numéro spécial. De grands défis et des solutions pour l'élevage
- Catherine HURTAUD, Rim CHAABOUNI, Rémi RESMOND, Guy MIRANDA, Benoît GRAULET, Clémence MORINIÈRE, Caractérisation du lait de deux races locales de vaches : la Bretonne Pie Noir et la Froment du Léon , INRAE Productions Animales: Vol. 34 No 1 (2021)
- Christian DUCROT, Maria Belén BARRIO, Alain BOISSY, François CHARRIER, Sergine EVEN, Pierre MORMÈDE, Sandrine PETIT, Marie-Hélène PINARD-VAN DER LAAN, François SCHELCHER, François CASABIANCA, Alain DUCOS, Gilles FOUCRAS, Raphaël GUATTEO, Jean-Louis PEYRAUD, Muriel VAYSSIER-TAUSSAT, Patrick VEYSSET, Nicolas C. FRIGGENS, Xavier FERNANDEZ, Améliorer conjointement la santé et le bien-être des animaux dans la transition des systèmes d’élevage vers la durabilité , INRAE Productions Animales: Vol. 37 No 3 (2024)
- Hervé GUYOMARD, Zohra BOUAMRA-MECHEMACHE, Vincent CHATELLIER, Luc DELABY, Cécile DÉTANG-DÉSSENDRE, Jean-Louis PEYRAUD, Vincent RÉQUILLART, Pourquoi et comment réguler la production et la consommation de produits animaux ? Le cas de l'Union européenne , INRAE Productions Animales: Vol. 34 No 3 (2021)
- Élisabeth BAÉZA-CAMPONE, Vincent CHATELLIER, Catherine HURTAUD, Anne FARRUGGIA, René BAUMONT, Avant-propos : Conséquences de la crise sanitaire de la Covid-19 sur les productions animales , INRAE Productions Animales: Vol. 34 No 4 (2021)
- René BAUMONT, Jean-Louis PEYRAUD, Avant-propos , INRAE Productions Animales: Vol. 28 No 1 (2015)

